
| A、水玻璃和石英的主要成份都是SiO2 |
| B、Al和Cu都是用还原法从它们的矿石中冶炼出来 |
| C、氧化铝陶瓷和氮化硅陶瓷都属于高温结构陶瓷 |
| D、常温下浓硫酸和浓硝酸都可贮存在铁制容器中 |


 核心素养学练评系列答案
核心素养学练评系列答案科目:高中化学 来源: 题型:
| A、9g D2O中含有的电子数目为5NA |
| B、1mol Na2O2中所含的阴离子数约为2×6.02×1023 |
| C、1mol CH4所含共价键总数为4NA |
| D、7.1g Cl2与足量NaOH溶液反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶液 | KOH | HNO3 | CH3COOH | HCl |
| 溶质质量分数ω(%) | 56 | 63 | 60 | 36.5 |
| 物质的量浓度c(mol/L) | 14.3 | 13.8 | 10.6 | 11.8 |
| A、HCl |
| B、HNO3 |
| C、CH3COOH |
| D、KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.56×10-3g |
| B、1.56×10-2g |
| C、7.8×10-4g |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸与Na2SiO3溶液混合:SiO32-+2H+═H2SiO3↓ | ||||
| B、往澄清石灰水中通入过量SO2:SO2+Ca2++2OH-═CaSO3↓+H2O | ||||
| C、NO2通入水中:H2O+3NO2═2H++2NO3-+NO | ||||
D、浓盐酸和二氧化锰共热制取Cl2:MnO2+4H++2Cl-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1催化剂450℃、1MPa |
| B、450℃、1MPa下,将1mol SO2和0.5molO2置于密闭的容器中充分反应生成SO3(g),放热98.5kJ,其热化学方程式为:2SO2+O2(g)?2 SO3(g)△H=-98.5kJ?mol-1 |
| C、氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH)2↓ |
| D、用FeCl3溶液腐蚀铜箔:Cu+2Fe3+═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
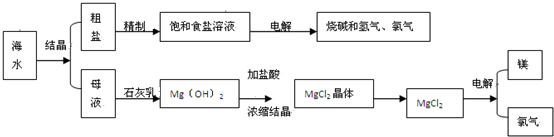
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com