
【题目】I、依据物质的分类标准可将一种物质归属多个类别。现有下列物质:
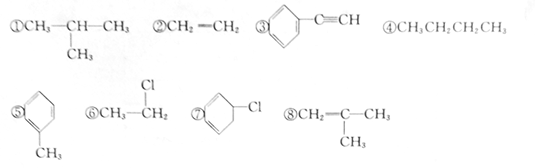
①属于卤代烃的有________ (填序号,下同)②属于烯烃的有________________
③属于同分异构体的有__________④属于芳香烃的有___________________
II、甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。
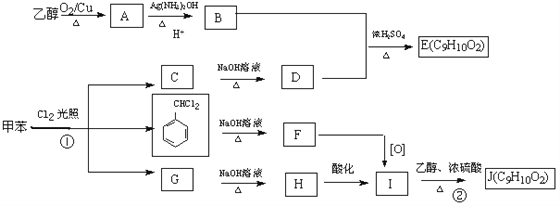
已知:
(1)写出F 的结构简式____________,其核磁共振氢谱图中有_____个吸收峰。
(2)写出D分子式____________,官能团名称____________。
(3)写出下列方程式,并注明反应类型。
① B+D→E: _____________________反应类型____________
② I→J :_____________________________
(4)E 、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式:
要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
①________________;②_______________;③______________;④______________。
【答案】 ⑥⑦ ②⑧ ①④ ③⑤ 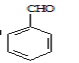 4 C7H8O (醇)羟基
4 C7H8O (醇)羟基 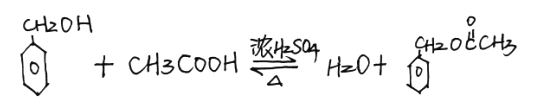 酯化反应(或取代反应)
酯化反应(或取代反应) 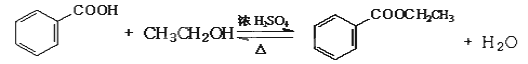

【解析】I、①属于卤代烃的有⑥⑦;②属于烯烃的有②⑧;③属于同分异构体的有①④;④属于芳香烃的有③⑤。
II、试题分析:乙醇经催化氧化生成A乙醛,A经银氨溶液氧化、再酸化生成B乙酸;甲苯与氯气在光照条件下发生侧链上的取代反应,由B和D的反应条件级B和E的分子组成,可以推断该反应为酯化反应;由B和E推出D为苯甲醇,C为甲苯侧链上的一氯代物;二氯代物在氢氧化钠溶液水解后,所得产物会自动脱水,所以F为苯甲醛;G只能是甲苯的三氯代物,其在碱性条件下水解的产物同样能自动脱水并与碱反应生成苯甲酸钠,酸化后转化为苯甲酸,I为苯甲酸与F的氧化产物相同;苯甲酸与乙醇发生酯化反应生成苯甲酸乙酯。
(1)F是苯甲醛,其结构简式为 ,其分子中有4种不同化学环境的H原子,所以其核磁共振氢谱图中有4个吸收峰。
,其分子中有4种不同化学环境的H原子,所以其核磁共振氢谱图中有4个吸收峰。
(2)D是苯甲醇,其分子式C7H8O,其官能团是(醇)羟基。
(3)① B+D→E的反应是酯化反应(属于取代反应),其化学方程式为: 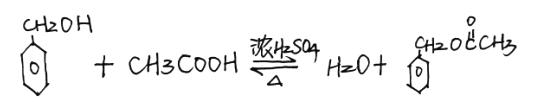
② I→J 的化学方程式为: 。
。
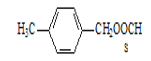
(4)E 、J有多种同分异构体,符合条件①与E、J属同类物质,即分子中有1个苯环和1个酯基;②苯环上有两个取代基且苯环上的一氯代物只有两种,则这两个取基在苯环上互为对位。此4种同分异构体的结构简式分别为:①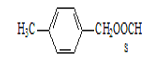 ;②
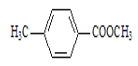
;② ;③
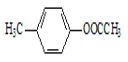
;③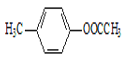 ;④
;④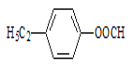 。
。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3, 下列对这四种气体的关系从大到小表达不正确的是
A. 体积②>③>①>④ B. 密度②>③>④>①
C. 质量②>③>①>④ D. 氢原子个数③>①>②>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学生设计的实验室制备干燥Cl2及吸收多余氯气的实验装置图,请回答:
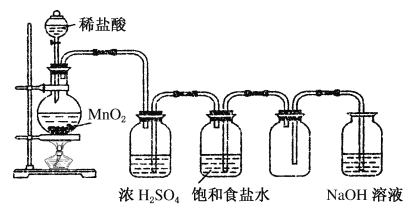
(1)指出上述图中的各处错误:
①_________________________________________________________;
②_________________________________________________________。
(2)在改过后的装置中,下列物质的作用分别是:
①饱和食盐水_________________________________________;
②浓硫酸____________________________________________;
③NaOH溶液_________________________________________。
(3)甲同学设计了如下图所示的实验装置并进行实验:
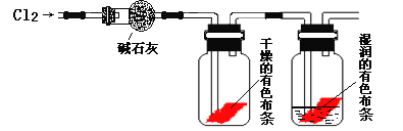
①甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因_____________________。
②甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是______________________________________,由此得出Cl2使有色物质褪色的机理是________________________________________;
(4)如果将过量二氧化锰与20mL12mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①_______________________,②_____________________________。
(5)为了提高浓盐酸的利用率,你对该实验的建议是___________________________________。
(6)写出圆底烧瓶中发生反应的离子方程式__________________________________________。
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是_________,有关的离子方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基准物质H2C2O4·2H2O的称量以及用NaOH溶液滴定等操作。下列有关说法正确的是( )
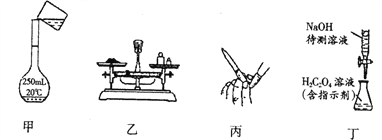
A. 用图甲所示操作转移NaOH溶液到容量瓶中
B. 用图乙所示装置准确称得2.21g H2C2O4·2H2O固体
C. 用图丙所示操作排除碱式滴定管中的气泡
D. 用图丁所示装置以NaOH待测液滴定H2C2O4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列实验操作或事故处理方法:① 用50 mL量筒量取5.0 mL硫酸铜溶液;② 称量没有腐蚀性固体药品时,把药品放在托盘上称量;③ 氢氧化钠浓溶液不慎溅入眼中,应立即用大量水冲洗,并且边洗边眨眼睛;④ 倾倒液体时,试剂瓶的瓶口不对准容器口;⑤ 块状药品都要用药匙取用;⑥ 固体药品用细口瓶保存;⑦ 用下图所示的方法闻气体的气味;⑧ 在实验中不慎手被玻璃划破,可用碘酒或双氧水清洗后,再用药外敷;⑨ 煤气中毒的人,立即进行人工呼吸;⑩ 浓H2SO4溅到皮肤上,用NaOH溶液中和。其中错误的是( )
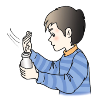
A. ①②③⑦⑨⑩ B. ③④⑩ C. ②⑤⑥⑦⑩ D. ①②④⑤⑥⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,温度不变时将某容器分隔成A,B两部分,A、B之间的挡板可以左右自由移动,B有可移动的活塞,在A中充入2molSO2和1molO2,平衡时A的体移变为原体积的0.7倍;在B中充入2molSO3和1molN2,在相同温度和任强条件下发生反应,也建立平衡。下列说法正确的是
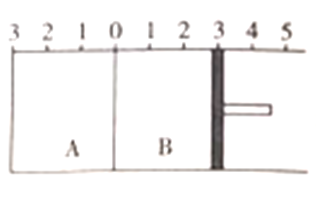
A. 平衡后A、B两容器的体积比大于2.1:3.1
B. 平衡后B容器中SO2的体积分数小于2/21
C. 平衡后B容器中SO3的转化率小于10%
D. 平衡后A、B两容器中S02的物质的量为A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是___________。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①___________,③___________。
(3)操作③中所用的有机试剂是CCl4,简述选择其理由_________________________________。
(4)操作过程③可以分解为如下几步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口玻璃塞是否漏液;
D. 倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液;
F. 从分液漏斗上口倒出上层水溶液;
G. 将分液漏斗上口的玻璃塞打开或使玻璃塞上的凹槽或小孔对准分液漏斗口上的小孔;
H. 静置、分层。
a.正确操作步骤的顺序是(填写各操作的编号字母):______→______→_____→A→____→G→E→F。_____
b.上述G步操作的目的是:_________________________________;
c.最后碘的有机溶液是通过___________获得(填“漏斗上口”或“漏斗下口”)。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___________________。
(6)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察下图所示实验装置,指出其所有错误之处__________________________________________。
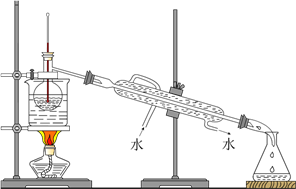
(7)进行上述蒸馏操作时,使用水浴的优点是_______________________________________,最后晶态碘在__________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1869年门捷列夫制作第一张周期表的根据是依据原子序数,这在当时有重要意义。
B.周期表中有七个主族,八个副族,一个0族。18个纵行,共16个族。
C.短周期元素是指1~20号元素。
D.周期表中有七个周期。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知食盐常加入KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:
KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
如果反应中转移0.2mol电子,则生成I2的物质的量为mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com