
【题目】在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3, 下列对这四种气体的关系从大到小表达不正确的是
A. 体积②>③>①>④ B. 密度②>③>④>①
C. 质量②>③>①>④ D. 氢原子个数③>①>②>④
【答案】D
【解析】
①标况下6.72LCH4的物质的量是6.72L÷22.4L·mol-1=0.3mol,质量是0.3mol×16g/mol=4.8g;
②3.01×1023个HCl分子物质的量为![]() =0.5mol,质量是0.5mol×36.5g/mol=18.25g;
=0.5mol,质量是0.5mol×36.5g/mol=18.25g;
③13.6g H2S物质的量为13.6g÷34g·mol-1=0.4mol;
④0.2mol NH3的质量是0.2mol×17g/mol=3.4g。则
A、同温同压条件下,气体的体积之比等于物质的量之比,所以体积②>③>①>④,A正确;
B、依据ρ=M/Vm可知,同温同压条件下,密度与摩尔质量成正比,甲烷:16g·mol-1,氯化氢:36.5g·mol-1,硫化氢34g·mol-1,氨气:17g·mol-1,所以密度②>③>④>①,B正确;
C、根据以上分析可知质量②>③>①>④,C正确;
D、①②③④中H原子物质的量分别是1.2mol、0.5mol、0.8mol、0.6mol,则氢原子个数大小顺序是①>③>④>②,D错误;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,并用单线桥法标出电子转移的方向和数目: ___________________________________________________________。该反应中,________是还原剂,________是还原产物,被还原的物质是________。
(2)在一定条件下,反应2NH3+3CuO![]() 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是______。
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是______。
①该反应是置换反应
②反应中NH3被氧化为N2
③在反应中体现了金属铜的还原性
④在反应中每生成1 mol H2O转移1 mol电子
(3)在反应2H2S+SO2![]() 3S+2H2O中被氧化的元素与被还原的元素的质量比为 ________。
3S+2H2O中被氧化的元素与被还原的元素的质量比为 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是_____,证明Fe3+存在的现象是__________。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:_________________。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

①请写出上述实验中③的化学式:_______
②配制并保存硫酸亚铁溶液时,常在其中加入_______________________
③要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为______。
①加入足量氯水 ②加入足量![]() 溶液 ③加入少量KSCN溶液
溶液 ③加入少量KSCN溶液
A、①③ B、③② C、③① D、①②③
④写出向②⑤的合并液中通入⑥的离子方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
I、(1)联氨分子的电子式为______________,
(2)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的方程式_______________。联氨与盐酸反应生成的正盐的化学方程式为__________________
II、某探究小组利用下列反应制取水合肼(N2H4·H2O):CO(NH2)2+2NaOH+NaClO===Na2CO3+N2H4·H2O+NaCl

实验一:制备NaClO溶液(实验装置如上图所示)
(1)配制30%NaOH溶液时,所需的玻璃仪器除量筒外,还有________(填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
实验二:制取水合肼(实验装置如右图所示)。

控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114 ℃馏分。(已知:N2H4·H2O+2NaClO===N2↑+3H2O+2NaCl)
(2)分液漏斗中的溶液是________(填标号)。
A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液
选择的理由是__________________________________________________
实验三:测定馏分中水合肼的含量。
称取馏分5.000 g,加入适量NaHCO3固体,加水配成250 mL溶液,移取25.00 mL,用0.100 0 mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5 左右。(已知:N2H4·H2O+2I2===N2↑+4HI+H2O)
(3)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_____________________。
(4)本实验用____________做指示剂,当滴定达到终点时的现象为_____________________。
(5)实验测得消耗I2溶液的平均值为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素A和B可形成组成为AB2的离子化合物,则A、B两原子的最外层电子排布分别为( )
A.ns2np2和ns2np4B.ns2和ns2np4C.ns2和ns2np5D.ns1和ns2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. PH=1的醋酸加水稀释到原体积的100倍,稀释后PH=3
B. 室温 pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性
C. 室温pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D. 某温度下,水的离子积常数为1×10-12,该温度下PH=7的溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.溴单质是深红棕色、密度比水小的液体
B.溴化银是一种重要的感光材料
C.工业上可用Cl2和石灰乳为原料制造漂白粉
D.碘化银可用于人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、依据物质的分类标准可将一种物质归属多个类别。现有下列物质:
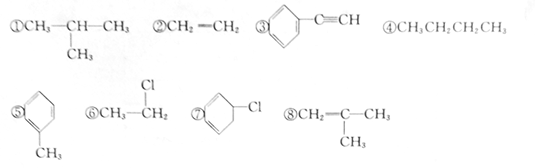
①属于卤代烃的有________ (填序号,下同)②属于烯烃的有________________
③属于同分异构体的有__________④属于芳香烃的有___________________
II、甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。
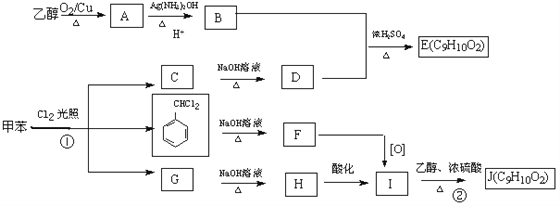
已知:
(1)写出F 的结构简式____________,其核磁共振氢谱图中有_____个吸收峰。
(2)写出D分子式____________,官能团名称____________。
(3)写出下列方程式,并注明反应类型。
① B+D→E: _____________________反应类型____________
② I→J :_____________________________
(4)E 、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式:
要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
①________________;②_______________;③______________;④______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com