
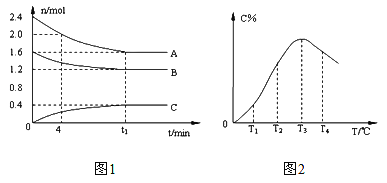
【题目】在10L定容密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2。下列分析不正确的是
A. t1时刻前,混合气体的密度减小,t1时刻后,混合气体的密度不变
B. 该反应的平衡常数表达式![]()
C. 由T1向T2变化时,V正> V逆
D. 此反应的正反应为放热反应
【答案】A
【解析】A,在恒容条件下,气体总体积不变、气体的总质量也不变,所以气体的密度也不变,所以A不正确。B,分析图1中数据可知,t1时刻反应达到化学平衡状态,从0~t1,A减少了0.8mol,B减少了0.4mol,C增加了0.4mol,因为变化量之比等于化学计量数之比,所以此反应的化学方程式为:2A(g) +B(g)![]() C(g),所以该反应的平衡常数表达式
C(g),所以该反应的平衡常数表达式![]() ,B正确。C,由图2可知,由T1向T2变化时,C的百分含量在增加,说明反应正在向正反应方向进行,所以V正> V逆,所以C正确。T3时C的百分含量达到最高,说明T3之前反应未达化学平衡状态,,T3之后,C的百分含量减少,说明温度升高化学平衡向逆反应方向移动,所以正反应为放热反应,D正确。
,B正确。C,由图2可知,由T1向T2变化时,C的百分含量在增加,说明反应正在向正反应方向进行,所以V正> V逆,所以C正确。T3时C的百分含量达到最高,说明T3之前反应未达化学平衡状态,,T3之后,C的百分含量减少,说明温度升高化学平衡向逆反应方向移动,所以正反应为放热反应,D正确。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质用途的叙述中正确的是( )
A.镁合金的硬度比镁小
B.推广使用无磷洗衣粉主要是为了防止水体富营养化
C.纯碱可作治疗胃酸过多的一种药剂
D.SO2可用于漂白一切有色物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中能大量共存的是
A.无色溶液中:K+、Na+、MnO4﹣、SO42﹣
B.在酸性溶液中:Mg2+、Na+、SO42﹣、Cl﹣
C.能使pH试纸变蓝色的溶液:Cl﹣、HCO3﹣、SO42﹣、NH4+
D.碱性溶液中:K+、Cl﹣、NO3﹣、Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期的主族元素,其原子序数依次增大。X元素形成的单质是自然界中含量最多的气体,Y是电负性最大的元素,W的原子最外层电子数与核外电子总数之比为3︰8,X的原子序数是Z的原子序数的一半,U是第四周期11列元素。
(1)U基态原子的价电子排布式__________________,Z在周期表中位置为___________________。
(2)在OY2中,氧原子的杂化轨道类型是____________。
(3)Z、W的最高价氧化物的水化物,酸性较强的是______。(填最高价氧化物的水化物的化学式)
(4)U的含氧化合物M晶胞如图所示(“○”表示氧原子),则M的化学式为________。
(5)已知:[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如右图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是( )

A.正极反应为AgCl +e-=Ag +Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减
少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的鉴别方法不正确的是( )
A.用焰色反应鉴别NaCl、KCl和K2SO4
B.用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液
C.利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液
D.用氯化钙溶液鉴别Na2CO3和NaHCO3两种溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com