
 C(g)+D(g)�����е������仯����ͼ��ʾ���жϸ÷�Ӧ��H 0 ���������������������ȷ��������
C(g)+D(g)�����е������仯����ͼ��ʾ���жϸ÷�Ӧ��H 0 ���������������������ȷ��������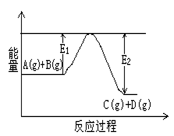
 O���Ȼ�ѧ����ʽΪ ��
O���Ȼ�ѧ����ʽΪ �� ����Һ̬˫��ˮ��H2O2����
����Һ̬˫��ˮ��H2O2����
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ϡ��Һ��������ͼӦ���к�����ֵ����� |
| B����ϡ��Һ��1mol���1mol�Ӧ�ų������������ |
| C����ϡ��Һ��HCl��NaOH��Ӧ���к�����HNO3��KOH��Ӧ���к�����ֵ��� |
| D����Ũ�����������������Һ�иպ�����1molˮʱ��������������Ϊ�к��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) ��H�� 0
CO(g) + H2(g) ��H�� 0  CO2(g) + H2��g�� ��H �� 0
CO2(g) + H2��g�� ��H �� 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ҫ���Ȳ��ܷ����ķ�Ӧ�����ȷ�Ӧ |
| B��ȼ�ϵ�ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ |
| C��ÿ����ѧ��Ӧ�������������ı仯 |
| D����ѧ��Ӧ�������仯�뷴Ӧ�������������������������й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��̼��ȼ�� | B���������������������ֽ� |
| C��Ba(OH)2��8H2O��NH4Cl��Ӧ | D��п����ϡH2SO4��Ӧ��ȡH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2O(g)��H2O(l)��H=" -44.0" KJ/mol |
B��2HI(g)��H2(g)��I2(g)��H= +1 4.9 KJ/mol 4.9 KJ/mol |
| C���γɻ�ѧ��ʱ���ų�����862KJ�Ļ�ѧ��Ӧ |
| D�������仯��ͼ��ʾ�Ļ�ѧ��Ӧ |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ����
����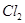 ������Ӧ����
������Ӧ����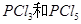 ����Ӧ���̺�������ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ����
����Ӧ���̺�������ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ���� ��������ݡ���֪
��������ݡ���֪ �ֽ�����
�ֽ����� ���÷ֽⷴӦ�ǿ��淴Ӧ������˵����ȷ����
���÷ֽⷴӦ�ǿ��淴Ӧ������˵����ȷ����
A�������������䣬�����¶������� ������ ������ |
B����Ӧ ��Ӧ�ķ�Ӧ�� ��Ӧ�ķ�Ӧ�� |
C�� ��Ӧ���� ��Ӧ���� ���Ȼ�ѧ����ʽΪ�� ���Ȼ�ѧ����ʽΪ��  |
D�������������䣬���� �ֽ����� �ֽ����� �ķ�Ӧ������ѹǿ�� �ķ�Ӧ������ѹǿ�� ��ת���ʼ�С��ƽ�ⳣ��K��С ��ת���ʼ�С��ƽ�ⳣ��K��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��920 kJ | B��557 kJ | C��436 kJ | D��188 kJ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com