
【题目】下表是中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题.
族 | IA | 0 | |||||||
1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
2 | ② | ③ | ⑥ | Ne | |||||
3 | ④ | ⑤ | Al | S | |||||
(1)⑥表示的元素是;
(2)②的原子结构示意图是;
(3)由①和③两种元素组成的化合物的化学式是;
(4)④和⑤两种元素的金属性强弱顺序是④⑤(填“<”或“>”).
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】四个化学小组的同学测定某Na2CO3固体样品(仅含NaCl杂质)的纯度,他们提出了各自的气体分析法。
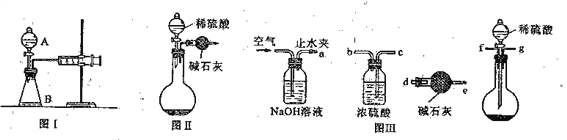
(1)第一小组用图I所示装置,仪器A的名称_____________。把m1g的混合物与足量稀硫酸反应后,测定产生CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是__________________________________________________________________________。
(2)第二小组用图装置测定CO2的质量。该装置存在明显缺陷是:__________________。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图Ⅲ,装置的连接顺序是a→____________________________________。(填写接口字母,图中仪器可重复使用)。实验中取了样品m1g,称量干燥管质量为m2g;与足量稀硫酸反应后称量干燥管质量为m3g,则Na2CO3的纯度表达式为__________________。
(4)第四小组设计用沉淀法来测定。方案是滴加沉淀剂使碳酸钠转化为沉淀,然后过滤、洗涤、干燥后称量沉淀质量。经讨论认为需要用Ba(OH)2液代替澄清石灰水Ca(OH)2来做沉淀剂其原因__________________(填入正确选项)。
a. Ba(OH)2比Ca(OH)2便宜
b. Ba(OH)2溶解度大于Ca(OH)2,可以增大Ba(OH)2浓度,无需加入过大体积的沉淀剂
c.相同条件下,CaCO3的溶解度明显小于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,互为同分异构体的是( )
A.CH3CH2CH2CH2CH3和CH3CH(CH3)2
B.CH2=C(CH3)2和CH2=CHCH=CH2
C.O2和O3
D.CH3CH2OH和CH3﹣O﹣CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛. 
(1)为了减缓海水对钢闸门A和C的腐蚀,图1中,材料B可以选择(填字母序号). a.锌板 b.铜板 c.碳棒
图2中,钢闸门C作极.若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极
反应式为 , 检测该电极反应产物的试剂是 .
(2)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图3所示(质子交换膜只允许H+自由通过).该电池的正极反应式为 .
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸(弱酸)的原理如图4所示(图中“HA”表示乳酸 分子,A﹣表示乳酸根离子).
①阳极的电极反应式为 .
②简述浓缩室中得到浓乳酸的原理: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物V L(标准状况下),溶于m g水中,得到质量分数为w 的溶液,物质的量浓度为c mol/L,密度为d g/mL,则下列说法不正确的是( )
A.相对分子质量 M= ![]()
B.物质的量浓度 c= ![]()
C.溶质的质量分数 w= ![]()
D.溶液密度 d= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:
①H2②铝③CaO④CO2⑤H2SO4 ⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
属于该类的物质 |
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为 .
(3)⑩在水中的电离方程式为 ,
(4)少量的④通入⑥的溶液中反应的离子方程式为 .
(5)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是(填化学式),氧化剂与还原剂的物质的量之比是 , 当有5.4gAl发生反应时,转移电子的物质的量为 . 该反应的离子方程式为 .
(6)白色沉淀变成灰绿色再变成红褐色沉淀的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是 .
A.c(H+)
B.![]()
C.c(H+)c(OH﹣)
D.![]()
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将(填“增大”、“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)pH(乙)(填“>”、“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)V(乙)( 填“>”、“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数K1 | 1.8×10﹣5 | 4.3×10﹣7 | 3.0×10﹣8 |
K2 | ﹣﹣ | 5.6×10﹣11 | ﹣﹣ |
下列四种离子结合H+能力最强的是 .
A.HCO ![]() B.CO
B.CO ![]() C.ClO﹣ D.CH3COO﹣
C.ClO﹣ D.CH3COO﹣
写出下列反应的离子方程式:CH3COOH+Na2CO3(少量):;HClO+Na2CO3(少量): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质俗名与化学式对应错误的是
A.胆矾 CuSO45H2O
B.重晶石 BaSO3
C.绿矾 FeSO47H2O
D.明矾KAl(SO4)212H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com