
【题目】关于下列化工生产流程的说法不正确的是
①铁矿石、焦炭、石灰石、空气、生铁
②黄铜矿![]() Cu2S
Cu2S![]() Cu(粗)
Cu(粗)![]() Cu(精)
Cu(精)
③石英![]() Si(粗)
Si(粗)![]() SiCl4
SiCl4![]() Si(高纯)
Si(高纯)
④![]()
A. ①的主要设备是炼铁高炉,生产过程中产生的高炉煤气主要成分是![]() 等,形成的炉渣中某成分可用作生产普通玻璃
等,形成的炉渣中某成分可用作生产普通玻璃
B. ②中电解精炼铜时,粗铜中的杂质全部沉积在阳极区,由![]() 组成的电解液需循环更换
组成的电解液需循环更换
C. ③中粗硅与![]() 反应后,可用分馏的方法提纯
反应后,可用分馏的方法提纯![]()
D. ④中Ⅰ、IV两步转化后的气体均需循环以提高原料的利用率
科目:高中化学 来源: 题型:
【题目】活性ZnO在橡胶、塑料、涂料工业有重要应用,工业上用含锌物料(含FeO、CuO等杂质)制取活性ZnO的流程如图所示:
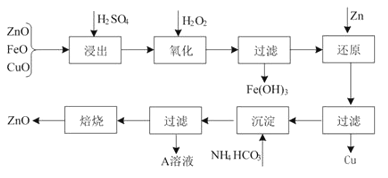
(1)上述流程中,浸出时用的是60% H2SO4(密度是1.5 g/cm3),则该H2SO4的物质的量浓度为______________ (保留两位小数) 。
(2)上述流程H2SO4浸出后溶液中Fe3+的浓度为0.04 mol·L-1,控制滤液的pH,加入H2O2后产生大量红褐色沉淀。
①粗略测定溶液pH的实验操作是___________________________________________。
②已知:常温下Fe(OH)3的Ksp=4.0×10-38。滤液的pH至少为________时,溶液中Fe3+开始沉淀。
(3)A溶液中主要含有的溶质是______________,验证溶质所含阳离子的方法是_____________。
(4)制备ZnO所焙烧的物质是含结晶水的碱式碳酸锌。取碱式碳酸锌6.82g,溶于HCl生成CO2 448 mL(标准状况下),溶解过程消耗HCl 0.12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是
A. 用干燥洁净的玻璃棒蘸取![]() 溶液,点到置于表面皿的pH试纸上测pH
溶液,点到置于表面皿的pH试纸上测pH
B. 氢氧化钠固体或碱石灰既可与浓氨水作用制得氨气,也可用于干燥氨气
C. 双氧水不稳定,见光、遇热、遇大多数金属氧化物都会加快它的分解,但在碱性环境下分解较慢
D. 海带中提取碘的过程中,可用过量的氯气或双氧水氧化水溶液中的![]() ,得到碘单质
,得到碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-="==" Cl-+ ClO-+ H2O
B. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O
D. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+CH3COO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是

A. 容器I、Ⅲ中平衡常数相同
B. 容器II、Ⅲ中正反应速率相同
C. SO3的体积分数:Ⅱ>III
D. 容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和大于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法错误的是( )
A.常温常压下,1mol甲烷分子中所含质子数为10NA
B.2mol/L的NaCl溶液中钠离数目为2NA
C.常温下,46gNO2和N2O4的混合气体中含有的氮原子数目为NA
D.若120g石墨能写a个字,则平均每个字的含有10NA/a个碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g) △H=-359.8kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-556.0kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出体现甲醇燃烧热的热化学方程式为________________________________。
(2)某温度时,将2 mol CO与5 mol H2的混合气体充入容积为2 L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。
CH3OH(g)。
①经过5 min后,反应达到平衡,此时转移电子6 mol。该反应的平衡常数为________。v(H2)=________ mol/(L·min)。若保持体积不变,再充入2 mol CO和1.5 mol CH3OH,此时v(正)________v(逆)(填“>”“<”或“=”)。
②在其他条件不变的情况下,再增加2 mol CO与5 mol H2,达到新平衡时,CO的转化率________(填“增大”“减小”或“不变”)。
③下列不能说明该反应已达到平衡状态的是________。
a.CH3OH的质量不变 b.混合气体的平均相对分子质量不再改变 c.v逆(CO)=2v正(H2) d.混合气体的密度不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯加水,则灯泡会亮起来:
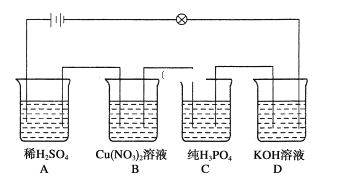
则:(1)加水的烧杯为__________。
(2)写出下列离子方程式:
硝酸铜溶液与氢氧化钾溶液混合_________,稀硫酸溶液与碳酸钠溶液混合_________
(3)若在A烧杯中加入Ba(OH)2溶液后,溶液的导电性________。(填“变强”“变弱”“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com