
某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究。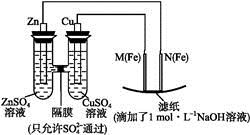

图1 图2
请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是 (填序号)。
| A.铝 | B.石墨 | C.银 | D.铂 |
 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。  )在溶液中呈紫红色。
)在溶液中呈紫红色。
 +4H2O和 。
+4H2O和 。  Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2
(1)A (2)2H++2e- H2↑(或2H2O+2e-
H2↑(或2H2O+2e- H2↑+2OH-)
H2↑+2OH-)
(3)从右向左 滤纸上M极附近有红褐色斑点产生(答出“红褐色斑点”或“红褐色沉淀”即可)
(4)增大 (5)4OH--4e- 2H2O+O2↑
2H2O+O2↑
(6)0.28 (7)2 +6e-+5H2O
+6e-+5H2O Fe2O3+10OH-
Fe2O3+10OH-
解析(1)铝与CuSO4溶液反应,且比Zn活泼;(2)N极为阴极,发生得电子反应,溶液中只有H+得电子;(3) 向负极(左)移动,滤纸上阴极有OH-生成、阳极有Fe2+生成,两离子生成白色Fe(OH)2沉淀,迅速变为灰绿色,最后变为红褐色;(4)X极是阴极,H+得电子,所以pH增大;(5)两极均有气体产生,可知阳极生成的气体只能是氧气;(6)X极收集n(H2)="0.03" mol,得0.06 mol电子,Y极收集n(O2)="0.007" 5 mol,OH-失去0.03 mol电子,所以参加反应的n(Fe)=
向负极(左)移动,滤纸上阴极有OH-生成、阳极有Fe2+生成,两离子生成白色Fe(OH)2沉淀,迅速变为灰绿色,最后变为红褐色;(4)X极是阴极,H+得电子,所以pH增大;(5)两极均有气体产生,可知阳极生成的气体只能是氧气;(6)X极收集n(H2)="0.03" mol,得0.06 mol电子,Y极收集n(O2)="0.007" 5 mol,OH-失去0.03 mol电子,所以参加反应的n(Fe)=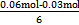 ="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2
="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2 +6e-
+6e-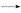 Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2
Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2 +6e-+5H2O
+6e-+5H2O Fe2O3+10OH-。
Fe2O3+10OH-。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
如图甲、乙是电化学实验装置。
(1)若甲、乙两烧杯中均盛有NaCl溶液,则:
①甲中石墨棒上的电极反应式为 ;
②乙中总反应的离子方程式为 ;
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2 。若反应中Cl2和I2的物质的量之比为5∶1,且 生成两种酸,该反应的化学方程式为 。
(2)若甲乙两烧杯中均盛有足量CuSO4溶液,则:
①甲中铁棒上的电极反应式为 ;
②如果起始时乙中盛有200mLpH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入的物质是 (写化学式),其质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)(Ⅰ)下列装置能组成原电池的是_____________ (填序号)
(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是,则不用回答)。
(1)正极材料是_______________________
(2)负极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)阴离子的移动方向___________________________________
(5)导线中电子的流向________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的 棒,乙装置中的 棒。
②乙装置中阳极的电极反应式是: 。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式: 。
②甲装置中碳极的电极反应式是 ,乙装置碳极的电极反应属于 (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64)。
按照实验步骤依次回答下列问题:
(1)导线中电子流向为__________________(用a、b表示)。
(2)写出装置中锌电极上的电极反应式:____________________________________;
(3)若装置中铜电极的质量增加0.64 g,则导线中转移的电子数目为________;(不许用“NA”表示)
(4)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
| A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动 |
| B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动 |
| C.盐桥中的K+、Cl-都向左侧烧杯移动 |
| D.盐桥中的K+、Cl-几乎都不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某兴趣小组为了提高电池的效率,设计了下图所示的原电池。
请回答下列问题:
(1)若X是AlCl3溶液,Y是稀硫酸,请你写出电极名称及电极反应:
Al片( ) ____________________________,
Cu片( ) ____________________________。
(2)若X是浓硝酸,Y是NaCl溶液,请你写出电极名称及电极反应:
Al片( ) ____________________________,
Cu片( ) ____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________。

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
①A电极对应的金属是________(写元素名称),B电极的电极反应式是________________________。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
____________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求写出计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是 (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应,正极: ;负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图:
回答下列问题:
(1)根据原电池原理填写下表:
| 装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
| 甲 | | | |
| 乙 | | | |
| 丙 | | | |
| 丁 | | | |
| 戊 | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com