
【题目】研究氮氧化物的反应机理,对于消除环境污染有重要意义。
(1)升高温度绝大多数的化学反应速率增大,但是2NO(g)+O2(g)![]() 2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
i:2NO(g)![]() N2O2(g)(快),v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0
N2O2(g)(快),v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0
ii:N2O2(g)+O2(g)![]() 2NO2(g)(慢),v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0
2NO2(g)(慢),v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0
请回答下列问题:
①一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=________
2NO2(g)达到衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=________
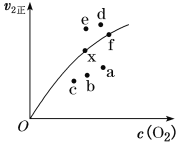
②由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为___________(填字母)。
(2)100℃时,若将0.100 mol N2O4气体放入1 L密闭容器中,发生反应N2O4(g)![]() 2NO2(g) ΔH=+24.4 kJ·mol-1。c(N2O4)随时间的变化如表所示。回答下列问题:
2NO2(g) ΔH=+24.4 kJ·mol-1。c(N2O4)随时间的变化如表所示。回答下列问题:

①在0~40 s时段,化学反应速率v(NO2)为______ mol·L-1·s-1
②下列能说明该反应达到平衡状态的是________(填选项字母)。
A.2v(N2O4)=v(NO2) B.体系的颜色不再改变
C.混合气体的密度不再改变 D.混合气体的压强不再改变
③该反应达到平衡后,若只改变一个条件,达到新平衡时,下列能使NO2的体积分数增大的是_________(填选项字母)。
A.充入一定量的NO2 B.增大容器的容积
C.分离出一定量的NO2 D.充入一定量的N2
④100℃时,若将9.2 g NO2和N2O4气体放入1 L密闭容器中,发生反应N2O4(g)![]() 2NO2(g)。某时刻测得容器内气体的平均相对分子质量为50,则此时v正(N2O4)_______v逆(N2O4)(填“>”“=”或“<”)。
2NO2(g)。某时刻测得容器内气体的平均相对分子质量为50,则此时v正(N2O4)_______v逆(N2O4)(填“>”“=”或“<”)。
⑤上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,若将一定量N2O4投入真空容器中恒温恒压分解(温度298 K、压强100 kPa),已知该条件下k正=4.8×104 s-1,当
【答案】![]() a 0.0025 BD BC < 3.9×106
a 0.0025 BD BC < 3.9×106
【解析】
(1)①由反应达平衡状态,所以![]() ,所以
,所以![]() ,
, ![]() ,据此分析;
,据此分析;
②![]() 的速率随温度的升高而减小,因为决定该反应速率的是反应②,故升高到温度时v2正减小,且平衡逆向移动,氧气的浓度增大;
的速率随温度的升高而减小,因为决定该反应速率的是反应②,故升高到温度时v2正减小,且平衡逆向移动,氧气的浓度增大;
(2)①![]() ,由反应速率之比等于化学计量数之比,则
,由反应速率之比等于化学计量数之比,则![]() ;
;
②平衡状态的判定;
③利用等效平衡思想解决;
④题干中给出的数据算出平均分子量=气体总质量气体总的物质的量=![]() =57.5g/mol,某时刻测得容器内气体的平均相对分子质量为50,说明反应需向体积缩小的方向进行;
=57.5g/mol,某时刻测得容器内气体的平均相对分子质量为50,说明反应需向体积缩小的方向进行;
⑤列三段式解出![]() 的分压,计算即可。
的分压,计算即可。
(1)①![]() ;②
;②![]() ;目标反应
;目标反应![]() ,由反应达平衡状态,所以
,由反应达平衡状态,所以![]() ,所以
,所以![]() ,
, ![]() ,则
,则![]() ,故答案为:
,故答案为:![]() ;
;
②![]() 的速率随温度的升高而减小,因为决定该反应速率的是反应②,故升高到温度时v2正减小,且平衡逆向移动,氧气的浓度增大,所以反应重新达到平衡,则变为相应的点为a,故答案为:a;
的速率随温度的升高而减小,因为决定该反应速率的是反应②,故升高到温度时v2正减小,且平衡逆向移动,氧气的浓度增大,所以反应重新达到平衡,则变为相应的点为a,故答案为:a;
(2)①由表可知,040s时间内![]() 的浓度由0.10mol/L减小为0.050mol/L,则其反应速率为
的浓度由0.10mol/L减小为0.050mol/L,则其反应速率为![]() ,由反应速率之比等于化学计量数之比,则
,由反应速率之比等于化学计量数之比,则![]() 的反应速率为
的反应速率为![]() ,故答案为:0.0025;
,故答案为:0.0025;
②A.未体现正逆反应速率的关系,A错误;
B.体系的颜色不再改变,说明二氧化氮的浓度不变,B正确;
C.无论是否反应,体系的混合气体的总质量不变,体积不变,故密度不变,C错误;
D.该反应正反应为体积增大的反应,混合气体的压强不再改变,说明气体的物质的量不变,达到平衡状态,D正确;
故答案为:BD;
③A. 充入一定量的![]() ,相当于加压,达新平衡时,则
,相当于加压,达新平衡时,则![]() 的体积分数减小,故A错误;
的体积分数减小,故A错误;
B. 增大容器的容积,减压,平衡向体积增大的方向移动,即正向移动,![]() 的体积分数增大,故B正确;
的体积分数增大,故B正确;
C. 分离出一定量的![]() ,相当于减压,使
,相当于减压,使![]() 的体积分数增大,故C正确;
的体积分数增大,故C正确;
D. 充入一定量的![]() ,总压增大,气体分压不变,不会引起化学平衡的移动,二氧化氮浓度不变,故D错误;
,总压增大,气体分压不变,不会引起化学平衡的移动,二氧化氮浓度不变,故D错误;
故答案为:BC;
④100℃时,将0.100mol![]() 气体放入1L密闭容器中,平衡时,
气体放入1L密闭容器中,平衡时,![]() ,
,![]() ,平均分子量=气体总质量气体总的物质的量=
,平均分子量=气体总质量气体总的物质的量=![]() =57.5g/mol,将9.2g
=57.5g/mol,将9.2g![]() 和
和![]() 气体放入1L密闭容器中,某时刻测得容器内气体的平均相对分子质量为50,说明反应需向体积缩小的方向进行,即
气体放入1L密闭容器中,某时刻测得容器内气体的平均相对分子质量为50,说明反应需向体积缩小的方向进行,即![]() ,故答案为:<;
,故答案为:<;
⑤当N2O4分解10%时,设投入的N2O4为1mol,转化的N2O4为0.1mol,则: ,故此时
,故此时![]() ,则
,则![]() ,故答案为:3.9×106。
,故答案为:3.9×106。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4=ZnSO4+H2↑,下列叙述正确的是
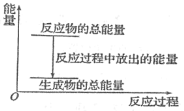
A.反应过程中的能量关系可用上图表示
B.1 mol Zn的能量大于1 mol H2的能量
C.若将其设计为原电池,则其能量转化形式为电能转化为化学能
D.若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的价电子排布式为____________,Y的电子排布图为___________;
(2)ZX2的分子式是________________,VSEPR模型名称为________________。YX2的电子式是______________,中心原子发生了________杂化。
(3)Y与Z形成的化合物的分子式是_______________。Y的氢化物中分子构型为正四面体的是_________(填名称),键角为______________,中心原子的杂化形式为_________。
(4)X的氢化物的沸点比同主族其他元素形成的氢化物沸点高,原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。充电时总反应为LiAO2 + nC = Li1-xAO2 + LixCn(0<x<1),工作原理如下图所示,则以下说法正确的是( )
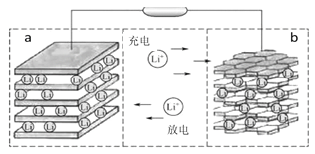
A. 放电时Ni元素最先失去电子
B. 放电时电子从a电极由导线移向b电极
C. 充电时的阳极反应式为LiAO2 - xe-= Li1-xAO2 + xLi+
D. 充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铬(CrCl3)为紫色晶体,在工业上主要用作媒染剂和催化剂,某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示。
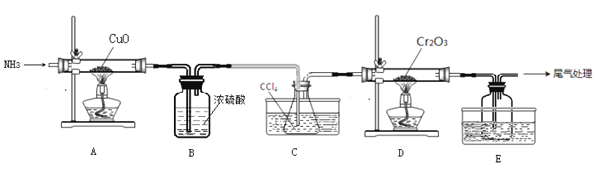
已知:①CrCl3熔点为83℃,易潮解,易升华,易溶于水但不易水解,高温下易被氧气氧化;②Cr2O3和CCl4在高温下反应的产物为CrCl3和光气(COCl2 )。请回答下列问题:
(1)装置A是氮气制备装置,氮气的作用是____________。
(2)装置B的作用为________。装置C和装置E的水槽中应分别盛有__________、____________。
(3)装置D中生成CrCl3和光气(COCl2 )的化学方程式为_________。
(4)该实验装置有设计不合理的地方,请写出改进方法:_________(写一点即可)
(5)产品中CrCl3质量分数的测定:
(i)称取0.3000 g得到的CrCl3样品溶于水并于250mL容量瓶中定容。
(ii)取25.00mL样品溶液于带塞的锥形瓶中,加热至沸腾后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的H2SO4酸化,将Cr3+氧化为Cr2O72-;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在
(iii)加入1mL指示剂,用0.0250 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL(已知2Na2S2O3+I2= Na2S4O6+2NaI)
①ii中加入稍过量的Na2O2后要加热煮沸,其主要原因是____________;加入KI发生反应的离子方程式为________________
②滴定实验可选用的指示剂为____________产品中CrCl3质量分数为_______%(结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg[c(H+)/c(OH-)]随加入NaOH的物质的量的变化如图所示。下列叙述正确的是( )
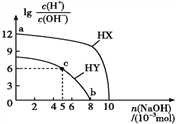
A. HX的酸性弱于HY B. c点溶液中:c(Y-)>c(HY)
C. a点由水电离出的c(H+)=10-12 mol·L-1 D. b点时酸碱恰好完全中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
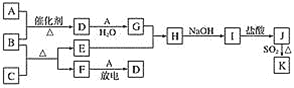
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是

A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气主要污染物,有效去除大气中的NOx是环境保护的重要课题。
(1)N2O又称笑气,有轻微的麻醉作用,N2O在一定条件下可分解为N2、O2。回答下列问题:
已知:①N2(g)+O2(g)=2NO(g) △H1=+180.5kJmol-1
②2NO(g)+O2(g)=2NO2(g) △H2=-114.14kJmol-1
③3NO(g)=N2O(g)+NO2(g) △H3=-115.52kJmol-1
则反应2N2O(g)=2N2(g)+O2(g) △H=_______ kJmol-1
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10molCO和8molNO发生反应,测得平衡时NO的体积分数与温度、压强的关系如下图

①已知T2>T1,则反应2NO(g)+2CO(g)![]() 2N2(g)+2CO2(g),△H___0(填“>”“=”或“<”)
2N2(g)+2CO2(g),△H___0(填“>”“=”或“<”)
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有____(填字母序号)
a.改用高效催化剂 b.缩小容器的体积 c.增加CO的浓度 d.升高温度
③压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,此时容器的体积为4L,则用N2的浓度变化表示的平均反应速率v(N2)=____,该温度下用分压表示的平衡常数Kp= ___MPa-1(分压=总压×物质的量分数)。
④在D点,对反应容器升温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中____点。
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。

①在50℃~150℃范围内随温度升高,NOx的去除率迅速上升的原因是____。
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com