
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑥ | | ⑦ | ⑨ | |
| 3 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 4 | ② | ④ | | | | | | |
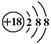 (2)氯 HClO4 (3)
(2)氯 HClO4 (3)
 。
。 。
。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.原子序数:Y>X>Z>W | B.离子半径: X+>Y2+>Z->W2- |
| C.原子最外层电子数:Z>W>Y>X | D.还原性: X>Y W2-> Z- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.四种元素位于同一周期 | B.氢化物的稳定性:H2Y>HZ |
| C.离子的氧化性:aW3+>bX+ | D.a+3=c-2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Y与Z形成的化合物是形成酸雨的原因之一 |
| B.W的单质能与水反应,生成一种具有漂白性的物质 |
| C.最高价氧化物对应水化物的酸性:W >Z >X |
| D.气态氢化物的稳定性:W > Z >Y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铊是易导电的银白色金属 | B.能生成+3价离子化合物 |
| C.T1(OH)3是两性氢氧化物 | D.Tl的失电子能力比Al强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:H2SiO3>H2CO3 | B.碱性:Mg(OH)2>Al(OH)3 |
| C.稳定性:SiH4>PH3 | D.原子半径:N>C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲与金属反应时得电子的数目比乙多 |
| B.甲单质的熔沸点比乙的低 |
| C.甲的氧化物对应的水化物酸性比乙强 |
| D.甲能将乙的简单离子从其盐溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -3 | -2 | +1 | -4 | -1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com