
| A、22.4L的HCl含有6.02×1023个粒子 |
| B、32g氧气中含有2mol的氧原子 |
| C、氢氧化钠的摩尔质量为40g |
| D、如果有6.02×1023颗大米,则这些大米的物质的量为1mol |
| m |
| M |


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
| A、NH3,O2 |
| B、H2O,O2 |
| C、CO2,O2 |
| D、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①③④ | D、③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4CNO和CO(NH2)2 |
| B、CuSO4?3H2O和CuSO4?5H2O |
C、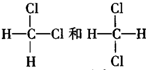 |
| D、H2O和D2O(重水) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蔗糖溶液中加入几滴稀硫酸,水浴加热5min,加入NaOH溶液至碱性,再加入银氨溶液并水浴加热检验葡萄糖的生成 |
| B、苯中混有苯酚可与足量氢氧化钠溶液反应后分液除去 |
| C、使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素 |
| D、只用溴水一种试剂即可鉴别甲苯、己烯、乙醇、四氯化碳四种液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
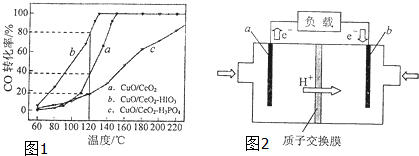
查看答案和解析>>
科目:高中化学 来源: 题型:
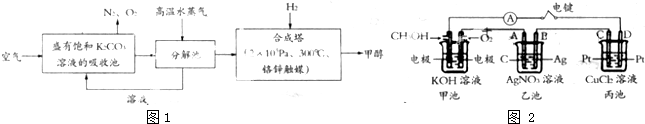
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com