
����Ŀ�������й�ʵ��IJ�����ԭ����������ȷ����![]()
A.��ȡ![]() ʱ����10g������������̣����������Ƶ�
ʱ����10g������������̣����������Ƶ�![]() ��λ��
���
B.������ˮ��Ӧ��ʵ��ʱ����ȡ�̶���С�Ľ����ƣ�����ֽ����������ú�ͣ������ձ��У��������η�̪��Һ���ټ�������ˮ��Ȼ��۲첢��¼ʵ������
C.���Թ��м���5mL��ˮ��2mL����![]() ���ۣ�������ã��۲��Թܵײ����ɺ�ɫ��״Һ��
���ۣ�������ã��۲��Թܵײ����ɺ�ɫ��״Һ��
D.Ϊ��֤���ŵ����ã��������ձ��зֱ�ʢ���������������Һ��ϡ���Ը��������Һ���������ʯī���õ����������������Ȼ����װ��![]() ������Һ����֬��U�����˲��������ձ��У�������ƫת��һ��ʱ�����������Һ��ɫ
������Һ����֬��U�����˲��������ձ��У�������ƫת��һ��ʱ�����������Һ��ɫ
���𰸡�D
��������
![]() ���������׳��⣬�и�ʴ�ԣ�����������Ӧ��������ȵ�С�ձ������Գ���ʱ��10g������������̵��ձ��ڣ���A����
���������׳��⣬�и�ʴ�ԣ�����������Ӧ��������ȵ�С�ձ������Գ���ʱ��10g������������̵��ձ��ڣ���A����
B.����˳�����Ӧ���ǽ��Ƽ�����˷�̪��ˮ�У�����Ӧ�ų��������ȣ���ˮ���ٶ������ձ�ը�ѣ���B����
C.��ˮ�뱽����Ӧ��Ӧ��Һ��ͱ��ڴ��������Ʊ��屽����C����
D.������������������������Һ��������ƫת˵�������˷�Ӧ������ͨ�������γɱպϻ�·����D��ȷ��
��ѡ��D��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��Ӧ�Ļ�ѧ����ʽΪA(g)��2B(g)![]() C(g)���ش��������⣺
C(g)���ش��������⣺
��1��ͼ1�Ƿ�ӦA(g)��2B(g)![]() C(g)�ڲ�ͬ�¶���A��ת������ʱ��仯�����ߡ�
C(g)�ڲ�ͬ�¶���A��ת������ʱ��仯�����ߡ�
�ٸ÷�Ӧ�ġ�H___(�>����<������)0��
��T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1___(�>����<������)K2����T1�¶��£������Ϊ1L���ܱ������У�����1molA(g)��2molB(g)�����A(g)��C(g)��Ũ����ʱ��仯��ͼ2��ʾ����÷�Ӧ��ƽ�ⳣ��Ϊ___��

���������ݻ����䣬���д�ʩ������Aת���ʵ���___(����ĸ)��
a.�����¶� b.��C(g)����ϵ�з���
c.ʹ�ú��ʵĴ��� d.����He��ʹ��ϵ��ѹǿ����
��2�����ݻ�Ϊ1L�ĺ����ܱ������У��ֱ��о���230��C��250���270�������µ�������Ӧ�������¶���B��A�����ʵ���֮����Aƽ��ת���ʵĹ�ϵ��ͼ3��ʾ������z��Ӧ���¶���___�棻���¶��£�����Ӧ��A�����ʵ���Ϊ1 mol����÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ___(�÷�����ʾ)��������a��b��c���Ӧ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2��K3����K1��K2��K3�Ĵ�С��ϵΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�![]() ��
��![]() ��������Һ����ʼʱ��Һ�����Ϊ
��������Һ����ʼʱ��Һ�����Ϊ![]() ���ֱ�������Һ�м�ˮ����ϡ�ͣ�ϡ�ͺ���Һ�����ΪV����ҺpH��
���ֱ�������Һ�м�ˮ����ϡ�ͣ�ϡ�ͺ���Һ�����ΪV����ҺpH��![]() �ı仯��ͼ��ʾ������˵����ȷ����
�ı仯��ͼ��ʾ������˵����ȷ����

A.�����ʵ���Ũ�ȵ�![]() ��
��![]() ��Һ�У�����ˮ�ĵ���̶ȴ�
��Һ�У�����ˮ�ĵ���̶ȴ�
B.��ϡ����![]() ʱ����������������к�
ʱ����������������к�![]()
C.������Һ��ϡ����![]() ʱ����Һ�У�
ʱ����Һ�У�![]()
D.![]() �ĵ��뷽��ʽ��
�ĵ��뷽��ʽ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t��ʱ��±������AgX��X=Cl��Br����2���ܽ�ƽ��������ͼ��ʾ����֪AgCl��AgBr��Ksp���μ�С����p(Ag+)=-lgc(Ag+)��p(X-)=-lgc(X-)������pX-pAg������ϵ�ɱ�ʾ��AgX���ܶȻ�����Һ�е�c(Ag+)��c(X-)�����ϵ������˵���������
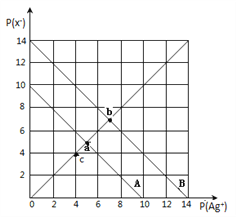
A. t��ʱ��c��ɱ�ʾAgCl�IJ�������Һ
B. B�߱�ʾ����AgBr
C. ȡa��b���㴦��Һ�������ϣ�ά��t�治�䣬�����Һ��һ���ް�ɫ��������
D. ��t��ʱ,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)ƽ�ⳣ��K��104
AgBr(s)+Cl-(aq)ƽ�ⳣ��K��104
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.��¯ˮ���е�![]() ������̼������Һ���ݿ�ת��Ϊ
������̼������Һ���ݿ�ת��Ϊ![]()
B.�����£��ں���![]() ��
��![]() ����Һ�У�
����Һ�У�![]() ��
��![]() Ũ��֮���Ǹ�����
Ũ��֮���Ǹ�����
C.������ﵽ����ƽ��ı�ij��������ƽ��������Ӧ�����ƶ�������Һ�ĵ�������һ����ǿ
D.��Ũ��Ϊ![]()
![]() ��HF��Һ��ˮ����ϡ�ͣ���Һ
��HF��Һ��ˮ����ϡ�ͣ���Һ![]() ʼ�ձ�������
ʼ�ձ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��2NO2(g)![]() 2NO(g)+O2(g)���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
2NO(g)+O2(g)���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2��ͬʱ������2n mol NO
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2:2:1��״̬
�ܻ���������ɫ���ٸı��״̬
�ݻ��������ܶȲ��ٸı��״̬
��������ƽ����Է����������ٸı��״̬
A. �٢ܢ�B. �ڢۢ�C. �٢ۢ�D. �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ص�ұ���ɲ������·�����2KF��CaC2![]() CaF2��2K����2C�������й�˵���������ǣ� ��
CaF2��2K����2C�������й�˵���������ǣ� ��
A���÷�Ӧ����������KF������������K
B���÷�Ӧ��˵��C�Ļ�ԭ�Դ���K
C�����KF��Һ�������Ʊ�������
D��CaC2��CaF2��Ϊ���ӻ���������������Ӹ����Ⱦ�Ϊ2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3��ˮ�ⷽ��ʽ��дΪFeCl3+3H2O![]() Fe(OH)3+3HCl�������ˮ��̶Ȳ�ȡ�ķ����� (������ )
Fe(OH)3+3HCl�������ˮ��̶Ȳ�ȡ�ķ����� (������ )
A.�����¶�B.��������Na2CO3 C.������������D.����FeCl3��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: 25�桢101 kPa�£��� 2 Na(s) + 1/2 O2(g) = Na2O(s) ��H1 = - 414 kJ / mol
�� 2 Na(s) + O2(g) = Na2O2(s) ��H2 = - 511 kJ / mol
����˵����ȷ����
A. ������������������Ӹ����Ȳ����
B. ���������ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C. ������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D. 25�桢101 kPa�£�Na2O2(s) + 2 Na(s) = 2 Na2O(s) ��H = -317 kJ / mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com