
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1 000 mL,其pH与溶液体积的关系如图19,下列说法正确的是( )
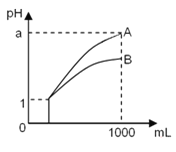
①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A.①④ B.②③ C.①③ D.②④
 核心素养学练评系列答案
核心素养学练评系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,在在恒容的密闭容器中,能表示反应X (g) + 2Y (g) ![]() 2Z (g)一定达到化学平衡状态的是:
2Z (g)一定达到化学平衡状态的是:
①X、Y、Z的物质的量之比为1:2:2
② X、Y、Z的浓度不再发生变化
③ 容器中的压强不再发生变化
④ 单位时间内生成n molZ,同时生成2n molY
A.①② B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面。查阅资料得到以下有关高氯酸的信息:
名称 | 分子式 | 外观 | 沸点 |
高氯酸 | HClO4 | 无色液体 | 130℃ |
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如下:

(1)操作①的名称是____________,操作②的名称是___________。
(2)反应器Ⅰ中发生反应的化学方程式为________________________。
(3)反应器Ⅱ中发生反应的离子方程式为__________________________。
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为___________。
(5)若想得到201kg的HClO4纯品,至少需要NaClO3_________kg。
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应N2(g)+3H2(g) ![]() 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A . N2,H2的和NH3的质量分数不再改变
B.c(N2):c(H2):c(NH3)=1:3:2
C .N2和H2的物质的量之和NH3的物质的量的2倍
D. 单位时间内每增加1molN2,同时增加3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
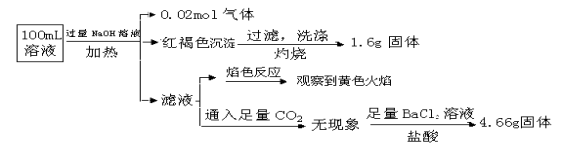
下列说法正确的是( )
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol·L-1
C.SO42ˉ、NH4+ 、Na+一定存在,CO32ˉ一定不存在
D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于H2S叙述不正确的是( )
A. H2S热稳定性差,在加热条件下会分解为硫单质与氢气
B. 部分金属硫化物不溶于酸,将硫化氢通入CuSO4、FeSO4等溶液中会出现黑色沉淀
C. H2S具有毒性,可以用湿润的醋酸铅试纸检验H2S
D. 久置的氢硫酸溶液易变质,是因为H2S具有很强的还原性,被空气中的O2氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com