
【题目】将2molNaHCO3和一定量的Na2O2固体混合,在加热的条件下使其反应,经测定无Na2O2剩余,则最后所得固体的物质的量(n)为
A.1mol<n≤2molB.1mol<n≤4molC.2mol<n≤4molD.n>4mol
【答案】B
【解析】
发生的反应方程式是:2NaHCO3![]() Na2CO3+CO2↑+H2O;2Na2O2+2H2O=4NaOH+ O2↑;2Na2O2+2CO2 =2Na2CO3+ O2。2molNaHCO3分解产生1mol的Na2CO3,1mol的CO2和1mol的H2O。CO2和H2O同时存在时,可以认为CO2先和Na2O2反应。若Na2O2不足量,产生的CO2没有完全消耗,此时固体的物质的量大于1mol;若Na2O2恰好完全与产生的CO2发生反应,则又产生固体Na2CO3的物质的量是1mol,此时所得固体的物质的量为2mol;若CO2反应完后还有Na2O2剩余,则Na2O2接着与水发生反应,若Na2O2和产生的1mol水完全反应,则产生的固体NaOH物质的量是2mol,此时反应后固体的总物质的量是4mol;所以反应后固体的物质的量介于1mol和4mol之间,因此选项是B。
Na2CO3+CO2↑+H2O;2Na2O2+2H2O=4NaOH+ O2↑;2Na2O2+2CO2 =2Na2CO3+ O2。2molNaHCO3分解产生1mol的Na2CO3,1mol的CO2和1mol的H2O。CO2和H2O同时存在时,可以认为CO2先和Na2O2反应。若Na2O2不足量,产生的CO2没有完全消耗,此时固体的物质的量大于1mol;若Na2O2恰好完全与产生的CO2发生反应,则又产生固体Na2CO3的物质的量是1mol,此时所得固体的物质的量为2mol;若CO2反应完后还有Na2O2剩余,则Na2O2接着与水发生反应,若Na2O2和产生的1mol水完全反应,则产生的固体NaOH物质的量是2mol,此时反应后固体的总物质的量是4mol;所以反应后固体的物质的量介于1mol和4mol之间,因此选项是B。


科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:X(g) + 3Y(g)![]() 2Z(g) ΔH < 0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所变化,但都没有改变各物质的初始加入量。下列说法正确的是( )
2Z(g) ΔH < 0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所变化,但都没有改变各物质的初始加入量。下列说法正确的是( )

A.t2时加入了催化剂B.t3时降低了温度
C.t5时增大了压强D.t4~t5时间内反应物转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题:
在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题:
(1)氯化铁溶液腐蚀铜板的离子方程式: ______ .
(2)将5至6滴饱和氯化铁溶液滴入到25mL沸水中,继续加热,得红褐色液体.
写出反应的离子方程式: ______ .
(3)向100mL![]() 硫酸铝铵
硫酸铝铵![]() 溶液中逐滴滴入
溶液中逐滴滴入![]()
![]() 溶液.随着
溶液.随着![]() 溶液体积V的变化,沉淀物质的量n的变化如图所示:
溶液体积V的变化,沉淀物质的量n的变化如图所示:
①请认真思考,写出相应的离子方程式:
OA段: ______
OB段: ______
BC段: ______
CD段: ______

②当![]() 离子恰好全部沉淀时,生成
离子恰好全部沉淀时,生成![]() 物质的量为 ______ mol.
物质的量为 ______ mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 25 ℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C. 在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol/L,则此时v正>v逆
D. 80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是工业上制取纯硅的一种方法。

请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有____(填反应代号);
(2)写出反应③的化学方程式____;
(3)化合物W的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至1 373~1 623 K反应,生成化合物W,其化学方程式是____;
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是___(填化学式);分别通入W溶液中能得到白色沉淀的气体是___(填化学式);
(5)工业上合成氨的原料H2的制法是先把焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H2,提纯水煤气得到纯净的H2的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)滴定终点的判断:溶液由_____________。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(_____)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为_________mL。

(4)某学生根据3次实验分别记录有关数据如表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
第一次 | 25.00 | 0.00 | 26.15 | ①V=__________ |
第二次 | 25.00 | 0.56 | 30.30 | |
第三次 | 25.00 | 0.20 | 26.35 | |
②依据上表数据计算该NaOH溶液的物质的量浓度________ (计算结果取4位有效数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向盐酸中加入氨水至中性,溶液中 >1
>1
B.醋酸溶液和氢氧化钠溶液恰好反应,溶液中![]() >1
>1![]()
C.向0.1molL-1CH3COOH溶液中加入少量水,溶液中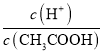 减小
减小
D.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com