
����Ŀ��ij�о�С��ͬѧͨ������������ȡ������ˮ��ϡ����ĻƼ������[KNH4Fex(SO4)y(OH)z]����ͨ��ʵ��ⶨ��Ʒ�лƼ���������й���ɡ�

ʵ��ⶨ��
����ȡһ����������Ʒ����ϡ�����г���ܽ⣬��������Һת��������ƿ�����Ƴ�l00mL��ҺA��
����ȡ25.00mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����9.32g��
����ȡ25.00mL��ҺA����������KI����2.000mol��L��1Na2S2O3��Һ���еζ�(��֪��ӦΪI2+2Na2S2O3�T2NaI+Na2S4O6������30.00mL Na2S2O3��Һ���յ㡣
(1)��[KNH4Fex(SO4)y(OH)z]��x��y��z�Ĵ�����ϵʽΪ ��
(2)������H2SO4��pH����Ϊ2������Һc(Fe3+)ӦΪ mol��L��1��(��֪Ksp[Fe(OH)3]��4.0��10��38)
(3)ʵ��ⶨ���м�������Ƿ���ȫ�ķ����� ��
(4)��������ʵ�����ݼ�����Ʒ�е�n(Fe3+)��n(SO42��)��(д���������)
���𰸡�(1)3x+2=2y+z (2)0.04 (3)���ã�ȡ���ɳ�������ϲ���Һ1-2ml���μ��������ữ���Ȼ�����Һ�����ް�ɫ�������ɣ��������������ȫ (4)3:2
��������
���������(1)��[KNH4Fex(SO4)y(OH)z]�У�KԪ�ػ��ϼ�+1�ۣ�NԪ�ػ��ϼ�-3�ۣ�HԪ�ػ��ϼ�+1�ۣ�SO42-���ϼ۴�����Ϊ-2�ۣ�OH-���ϼ۴�����Ϊ-1�ۣ�+1+(-3)+(+1)��4++3x+(-2y)+(-1��z)=0��x��y��z�Ĵ�����ϵʽΪ��3x+2=2y+z��
(2)������H2SO4��pH����Ϊ2��c(OH-)=![]() =10-12mol/L��Ksp[Fe(OH)3])=4.0x10-38=c(Fe3+)c3(OH-)��c(Fe3+)=
=10-12mol/L��Ksp[Fe(OH)3])=4.0x10-38=c(Fe3+)c3(OH-)��c(Fe3+)=![]() =0.04mol/L��
=0.04mol/L��
(3)ʵ��ⶨ������������Ƿ���ȫ�ķ����ǣ����ã�ȡ���ɳ�������ϲ���Һ1-2ml���μ��������ữ���Ȼ�����Һ�����ް�ɫ�������ɣ��������������ȫ��
(4)����ȡһ����������Ʒ����ϡ�����г���ܽ⣬��������Һת��������ƿ�����Ƴ�l00.00mL ��ҺA������ȡ25.00mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����9.32g������ȡ25.00mL��ҺA����������KI����2.000molL-1Na2S2O3��Һ���еζ�(��֪��ӦΪI2+2Na2S2O3�T2NaI+Na2S4O6������30.00mL Na2S2O3��Һ���յ���25ml��Һ��������������ʵ��������ᱵ���ʵ�����ͬ��n(SO42-)=n(BaSO4)=![]() =0.04mol��
=0.04mol��
2Fe3+��I2��2Na2S2O3
2 1 2
n(Fe3+)=2n(I2)=n(Na2S2O3)=2.000mol/L��0.03L=0.06mol��
��Ʒ�е�n(Fe3+)��n(SO42-)=0.06mol��0.04mol=3��2��


 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ������Ԫ���⣬������Ԫ�ص�����ϼ�����ֵ�϶����ڸ�Ԫ��������������
B. ��������С�ĵ����������
C. ͬ��s�ܼ����ڲ�ͬ�ĵ��Ӳ����������ɵ����������Dz���ͬ��
D. ��������Ų���ȫ��ͬ�����������仯ѧ����һ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����CH3OH��g��+3/2O2��g��=CO2��g��+2H2O��g����H=��akJ��molһ1
��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=��bkJ��molһ1
��CH4��g��+2O2��g��=CO2��g��+2H2O��1����H=��ckJ��molһ1
������������ȷ����
A���������Ȼ�ѧ����ʽ��֪b>c
B�������ȼ����ΪbkJ/mol
C��2CH3OH��g��=2CH4��g�� +O2��g�� ��H=2��bһa��KJ molһ1
D�����״��ͼ������ʵ���֮��Ϊ1:2ʱ������ȫȼ������CO2��H2O��1��ʱ���ų�������ΪQ kJ����û�����м״������ʵ���ΪQ/��a+2b�� mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������G�������ϳɺ���ı���ǰ�����ʣ��Ի������߹��ܺ���������Ҫ���á�������G ��һ�ֺϳ�·�����£�
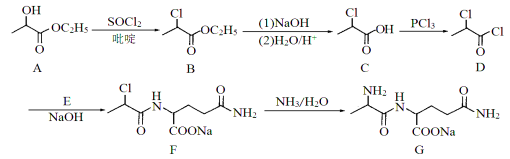
(1)������A�к��������ŵ�����Ϊ �� ��
(2)������E�ķ���ʽΪC5H10O3N2����ṹ��ʽΪ ����F��G�ķ�Ӧ����Ϊ ��
(3)һ��������F��ת��ΪH(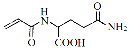 )��д��ͬʱ��������������H��һ��ͬ���칹��Ľṹ��ʽ ��
)��д��ͬʱ��������������H��һ��ͬ���칹��Ľṹ��ʽ ��
������FeCl3��Һ������ɫ��Ӧ�� ���������ᷴӦ�� ��������ֻ����3�ֲ�ͬ��ѧ����������
(4)��֪����![]() ��
��![]() �������
����д����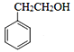 Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)��
�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬ�¶��£������Ϊ1 L���ĸ��ܱ������У������¶Ⱥ��ݻ����䣬�����ֲ�ͬ��Ͷ�Ϸ�ʽ���з�Ӧ��ƽ��ʱ�й�������������֪2SO2��g����O2��g�� ![]() 2SO3��g����H����196.6 kJ��mol��1����
2SO3��g����H����196.6 kJ��mol��1����
���� | �� | �� | �� | �� |
��ʼͶ���� | 2molSO2 1mol O2 | 1 mol SO2 0.5mol O2 | 2mol SO3 | 2mol SO2 2mol O2 |
��Ӧ�ų������յ�������kJ�� | a | b | c | d |
ƽ��ʱc��SO3�� ��mol��L��1�� | e | f | g | h |
���й�ϵ��ȷ������ ��
A��a��c��e��g B��a>2b��e>2f C��a>d��e>h D��c��98.3e>196.6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʽṹ�����ʡ��ѱ���Ϊ�������������������������������Ҫ�Ľṹ���ϡ�
(1)��̬��ԭ�ӵĺ�������Ų�ʽ�� ��
(2)���ʯ(TiO2)���۵�1825���������η�ֱ�ӵ����ʯ�ɻ�ý����ѣ����ʯ�����ľ��������� ���塣
(3)TiCl4����NH4Cl��Ӧ���������(NH4)2[TiCl6]��
����������У��γ���λ��ʱ�ṩ�¶Ե��ӵ��� ��(��Ԫ�ط���)
����NH4����Ϊ�ȵ������һ��������Ϊ ��(�ѧʽ)
(4)TiO2+��H2O2��ϡ���з�Ӧ�����ٺ�ɫ��[TiO(H2O2)]2+���ӣ��������ѵĶ��Լ��顣���й���H2O2��˵����ȷ���� ��(�����)
A���ռ乹��Ϊֱ���� |
B�����Ǽ��Լ��ļ��Է��� |
C��Oԭ�ӹ���ӻ�����Ϊsp3 |
D����ѧ���ʲ��ȶ�����Ϊ����ļ��ܽ�С |
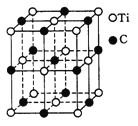
(5)�������һ������(Ti)ԭ�Ӻ�̼ԭ�ӹ��ɵ���̬�Ŵط��ӣ��ṹģ����ͼ��ʾ�����ķ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦA2(g)+2B2(g) ![]() 2AB2(g)��H��0������˵����ȷ����( )
2AB2(g)��H��0������˵����ȷ����( )
A�������¶ȣ�����Ӧ�������ӣ�����Ӧ���ʼ�С
B�������¶������ڷ�Ӧ�������ӣ��Ӷ����̴ﵽƽ���ʱ��
C���ﵽƽ��������¶Ȼ�����ѹǿ�������ڸ÷�Ӧƽ�������ƶ�
D���ﵽƽ������¶Ȼ��Сѹǿ�������ڸ÷�Ӧƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ------ѡ��3�����ʽṹ������]
M��R��X��YΪԭ��������������Ķ���������Ԫ�أ�Z��һ�ֹ���Ԫ�ء�M��̬ԭ��L����p�����������s�����������2����R��ͬ����Ԫ��������õĽ���Ԫ�أ�X��M�γɵ�һ�ֻ������������������Ҫ������Ⱦ�Z�Ļ�̬ԭ��4s��3d������������ش��������⣺
��1��R��̬ԭ�ӵĵ����Ų�ʽ�� ��X��Y�е縺�Խϴ���� (��Ԫ�ط���)��
��2��X���⻯��ķе��������������Ƶ�M���⻯���ԭ����___________��
��3��X��M�γɵ�XM3���ӵĿռ乹����__________��
��4��M��R���γɵ�һ�����ӻ�����R2M����ľ�����ͼ��ʾ��
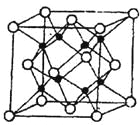
��ͼ�к��������������_________(�����ӷ���)�������ӵ���λ��Ϊ ���þ�������a="b=c=d" pm ����ʽ����R2M������ܶ�Ϊ g/cm��
��5����ϡ�����У�Z����ۺ�����ļ���(��ɫ)����M��һ���⻯�Z����ԭΪ+3�ۣ��÷�Ӧ�Ļ�ѧ����ʽ��__________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com