
【题目】[化学------选修3:物质结构与性质]
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是 ,X和Y中电负性较大的是 (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________。
(3)X与M形成的XM3分子的空间构型是__________。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,
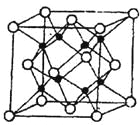
则图中黑球代表的离子是_________(填离子符号),该离子的配位数为 。该晶胞参数a="b=c=d" pm ,列式计算R2M晶体的密度为 g/cm。
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是__________。
【答案】(1)1s22s22p63s1;Cl
(2)H2O分子能形成氢键,而H2S不能形成氢键(3)平面三角形
(4)Na+;4;(4×62)÷[NA×(d×10-10)3]
(5)3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4
【解析】试题分析:M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,核外电子排布式为1s22s22p4,故M为O元素;由原子序数可知R、X、Y均处于第三周期,R是同周期元素中最活泼的金属元素,则R为Na;X和M形成的一种化合物是引起酸雨的主要大气污染物,则X为S元素,可知Y为Cl;Z的基态原子4s和3d轨道半充满,外围电子排布式为3d54s1,处于VIB族,故Z为Cr.
(1)R为Na,基态原子的电子排布式是1s22s22p63s1,同周期自左而右电负性增大,故Cl元素电负性大于S的;
(2)H2O分子能形成氢键,使水的沸点升高,而H2S不能形成氢键,故硫化氢的沸点低于水的;
(3)X与M形成的SO3分子中S原子孤电子对数=(6-2×3)÷2=0,价层电子对数为3+0=3,故其空间构型为平面三角形;
(4)M和R所形成的一种离子化合物为Na2O,晶胞中黑色球数目为8,白色球数目为8×1/8+6×1/2=4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+;Na+的配位数为4,晶胞相当于4个Na2O,晶胞参数a="b=c=d" pm,晶体的体积为(d×10-10)3cm,则晶体的密度为m/V=(4×62)÷[NA×(d×10-10)3]g/cm。
(5)Z的最高价含氧酸的钾盐(橙色)为K2Cr2O7,与氧元素的氢化物发生氧化还原反应,该氢化物为H2O2,在稀硫酸中,Cr元素被还原为+3价,H2O2被氧化生成氧气,反应方程式为:3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】某研究小组同学通过下列流程制取不溶于水和稀硫酸的黄钾铵铁矾[KNH4Fex(SO4)y(OH)z],并通过实验测定样品中黄钾铵铁矾的有关组成。

实验测定:
①称取一定质量的样品加入稀盐酸中充分溶解,将所得溶液转移至容量瓶并配制成l00mL溶液A;
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32g;
③量取25.00mL溶液A,加入足量KI,用2.000mol·L﹣1Na2S2O3溶液进行滴定(已知反应为I2+2Na2S2O3═2NaI+Na2S4O6,消耗30.00mL Na2S2O3溶液至终点。
(1)在[KNH4Fex(SO4)y(OH)z]中x、y、z的代数关系式为 。
(2)若加入H2SO4将pH调节为2,则溶液c(Fe3+)应为 mol·L﹣1。(已知Ksp[Fe(OH)3]=4.0×10﹣38)
(3)实验测定②中检验沉淀是否完全的方法是 。
(4)根据以上实验数据计算样品中的n(Fe3+)∶n(SO42﹣)。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,下列说法正确的是( )
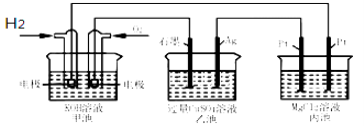
A.甲池通入O2的电极反应为O2 + 4e-+ 4H+=2H2O
B.乙池 Ag电极增重6.4g,溶液中将转移0.2mol电子
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A. 分散质颗粒直径都在1~100 nm之间
B. 加热蒸干、灼烧后都有氧化铁生成
C. 呈红褐色
D. 能透过半透膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关摩尔的使用正确的是( )
A.1mol O的质量为16g·mol-1
B.0.5mol He约含有6.02×1023个电子
C.2H既表示2个氢原子又表示2mol氢原子
D.每摩尔物质均含有6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液pH>7,用离子方程式表示原因_____________________。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的作用是_________________。
(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。向饱和NaClO溶液中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是_______________________。
(4)常温下,pH=11的NaClO溶液中,水电离出来的c(OH-)=________,在pH=3的HClO溶液中,水电离出来的c(H+)=____________________________。
(5)已知纯水中存在如下平衡:H2O+H2O![]() H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母)。
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母)。
A.向水中加入NaHSO4固体
B.向水中加Na2CO3固体
C.加热至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.向水中加入(NH4)2SO4固体
(6)若将等pH、等体积的②NaOH溶液和⑦NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m________n(填“<”、“>”或“=”)。
(7) 在25 ℃时,将0.2 mol NaA晶体和0.1 mol HA气体同时溶解于同一烧杯的水中,制得1 L溶液,则c(HA)+c(A-)= mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com