
����Ŀ�������йط�Ӧ�ȵ���������ȷ���ǣ� ��
���±����ݿ��Լ���� 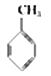 ��g��+3H2��g����
��g��+3H2��g���� 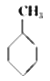 ��g���ķ�Ӧ�ȣ�
��g���ķ�Ӧ�ȣ�
���ۼ� | C��C | C�TC | C��H | H��H |
����/��kJmol��1�� | 348 | 610 | 413 | 436 |
����֪2H2��g��+O2��g���T2H2O��g����H=��483.6kJmol��1�� ��������ȼ����Ϊ��H=��241.8kJmol��1
���ɵ���Aת��Ϊ����B��һ�����ȹ��̣��ɴ˿�֪����B�ȵ���A�ȶ�
��X��g��+Y��g���TZ��g��+W��s����H��0�����º��������´ﵽƽ������X��������Ӧ�ġ�H����
���ɸ�˹���ɣ���֪����ͬ�����£����ʯ��ʯīȼ������1molCO2����ʱ���ų���������ȣ�
��25�棬101kPaʱ��1mol̼��ȫȼ������CO2���ų�������Ϊ̼��ȼ���ȣ�
A. �٢ڢۢ� B. �ۢܢ� C. �ܢ� D. ��
���𰸡�D
���������ٱ����в�����̼̼˫����̼̼���������ܼ��㷴Ӧ�ȣ��ٴ���������ˮ����̬������Һ̬�����ܼ���������ȼ���ȣ��ڴ����ɵ���Aת��Ϊ����B��һ�����ȹ��̣�˵��A������������B���ɴ˿�֪����A�ȵ���B�ȶ����۴��ܷ�Ӧ���뷴Ӧ������û�й�ϵ���ܴ��ݽ��ʯ��ʯī���е���������ͬ������ȼ������1molCO2����ʱ���ų�����������ȣ��ݴ���25�棬101kPaʱ��1mol̼��ȫȼ������CO2���ų�������Ϊ̼��ȼ���ȣ�����ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪CuCl2��Һ���Ҷ���H2N-CH2CH2-NH2[����(en)��ʾ]����,���γ�������(��ͼ��ʾ):

��ش���������U
���Ҷ���������Nԭ�ӳɼ�ʱ��ȡ���ӻ�������____________,
�Ҷ����е����Cl-CH2CH2-Cl����Ҫԭ����___________________________��
�������������к��еĻ�ѧ��������:__________________��(��д����,��ѡ) ;
a��λ�� b���Լ� c�Ǽ��Լ� d���Ӽ�
�۸������ [Cu(en)2]Cl2��ϵͳ����Ϊ_______;����ͭ���ӵ���λ����_______��
��2���±���ʵ����Ԫ�����ڱ��IJ��ֱ߽�,�����ϱ߽�δ��ʵ�߱����

������Ϣ�ش���������:
�����ڱ��л�̬Gaԭ�ӵ����������Ų�ʽΪ__________________
��FeԪ��λ�����ڱ���_____��;Fe��CO���γ������Fe(CO)5,��Fe(CO)5�����Ļ��ϼ�Ϊ____;
��֪:ԭ����Ŀ�͵�������(��۵�������)��ͬ�����ӻ�Ϊ�ȵ�����,�ȵ�����������ƵĽṹ��������CO���ӻ�Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ______��______(�ѧʽ)��
�۸���VSEPR����Ԥ��ED4-���ӵĿռ乹��Ϊ_________��B��C��D��Eԭ��������γɵķ�����,����ԭ�Ӷ����������8�����ȶ��ṹ�Ļ�ѧʽΪ____________(д2��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I ������þ���ʻ��ã������������ʷ�Ӧ��ijУ����С�����þ���ڶ�����̼��ȼ�գ��Ʋ�MgҲ����NO2ȼ�գ����ܲ���ΪMgO��N2��Mg3N2��ͨ����ͼ��ʾʵ��װ������֤��Ӧ����г�װ��ʡ�ԣ������������ظ�ʹ�ã�����֪��NO2�����ܱ�NaOH���գ�Mg3N2������ˮ��Ӧ��
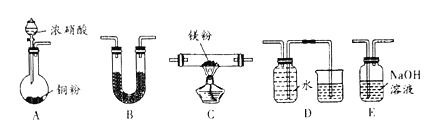
��1��ʵ���У�װ������������˳��ΪA _________������ĸ��ţ���װ��B ��������______��
��2����������N2��ʵ��װ��Ϊ__________������ĸ��ţ���
��3�����ʵ��֤���������д���Mg3N2 ____________��
��ҵ������þ��Ϊԭ�ϣ���Ҫ�ɷ�ΪMgCO3������SiO2��FeCO3�����ʣ��Ʊ���������þ��
��4�����ݷ�Ӧ����Ҫ���ȳ�ȥFeCO3������������������ķ��������м���H2O2ʱ��������Ӧ�����ӷ���ʽΪ__________��
��5����֪����һ��������CO(NH2)2����H2O��Ӧ����CO2��һ��������̺��ڣ���������ɺ��ټ���CO(NH2)2 ��ʼ����Mg2+���ù����з�����������Ҫ��ӦΪ���û�ѧ����ʽ�����ӷ�Ӧ����ʽ��ʾ��___________��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ����(N2H4��H2O)����ˮ����������ɫ�������и�ʴ�Ժ�ǿ��ԭ�Եļ���Һ�壬����һ����Ҫ�Ļ����Լ����������ط�����ˮ���µ�ԭ��Ϊ��
CO(NH2)2+2NaOH+NaC1O==N2H4��H2O+Na2CO3+NaCl��

ʵ��1���Ʊ�NaClO��Һ������֪��3NaClO![]() 2NaCl+NaClO3��
2NaCl+NaClO3��
(1)ͼ��װ��I����ƿ�ڷ�����Ӧ�Ļ�ѧ����ʽΪ_______________________��
(2)��NaOH��������������������Ϊ30��NaOH��Һʱ�����貣����������Ͳ���________________��(����)
a���ձ� b������ƿ c�������� d����ƿ
(3)ͼ��װ�â����ñ�ˮԡ�����¶ȵ�Ŀ����_________________��
ʵ��2����ȡˮ���¡�
(4)ͼ��������Һ©����Һ�ٶȹ��죬����N2H4��H2O�����A�з�Ӧ�������������������Ͳ�Ʒ���ʡ�д���ù��̷�Ӧ���ɵ����Ļ�ѧ����ʽ��________________________����ַ�Ӧ������A����Һ���ɵõ�ˮ���µĴֲ�Ʒ��
ʵ��3���ⶨ�����ˮ���µĺ�����
(5)��ȡ���3.0g����������NaHCO3����(�ζ������У�������Һ��pH������6��5����)����ˮ���250mL��Һ���Ƴ�25��00mL������ƿ�У����μ�2��3�ε�����Һ����0.15 mol��L-1�ĵ�ı���Һ�ζ���(��֪��N2H4��H2O+2I2==N2��+4HI+H2O)
�ٵζ�ʱ����ı���Һʢ����________(���ʽ����ʽ��)�ζ��ܡ�
�������ܵ��������ˮ���µĺ����ⶨ���ƫ�ߵ���_________��(����)
a����ƿ��ϴ�ɾ���δ����
b���ζ�ǰ���ζ����������ݣ��ζ���������
c������ʱ���ζ�ǰƽ�ӣ��ζ�����
d��ʢ��Һ�ĵζ���ˮϴ��ֱ��װ��Һ
��ʵ��������I2��Һ��ƽ��ֵΪ20��00mL�������ˮ����(N2H4��H2O)����������Ϊ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ի�����Ϊԭ�����������������ķ������������÷������Լ��ٻ�����Ⱦ�����Ϊ������ҵ�����÷���(��Fe2����Fe3���������μ�����CaO��MgO)�Ʊ��ߵ���������(Fe2O3)�ͻ���(NH4)2SO4�����������������£�

(1)�ڷ����ܽ����ʱ��Ӧѡ��________�ܽ�(����ĸ)��
A����ˮ B������������Һ C������ D������
(2) Ϊ����߷����Ľ�ȡ�ʣ��ɲ��õĴ�ʩ����Щ��_______________������д�����㣩��

(3)����A��һ������������ҵ�����ѡ��________(��ѡ��ʹ�õ��У�������Cl2��MnO2)����������_______________�����������з�����Ӧ�����ӷ���ʽΪ_________________��
(4)������ͼ�й����ݣ�����Ϊ��ҵ����������ʱӦ���Ƶ�����(���¶ȡ�pH������ʱ��������˵��)�ǣ�______________________________________________________��
(5) 炙������п��ܻ��е�������Fe(OH)3��________��
(6) 炙������Ļ�ѧʽ�ɱ�ʾΪ(NH4)xFey(SO4)z(OH)w���仯ѧʽ��ͨ������ʵ��ⶨ��
�� ��ȡһ����������Ʒ����ϡ�������ܽ⣬��������Һת��������ƿ�����Ƴ�100.00 mL��ҺA��
�� ��ȡ25.00 mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����9.32 g��
�� ��ȡ25.00 mL��ҺA����������NaOH��Һ�����ȣ��ռ�����״��������448mL��ͬʱ�к��ɫ�������ɡ�
�� �����������ó������ˡ�ϴ�ӡ����գ����յù���4.80 g��
ͨ�����㣬��ȷ��炙������Ļ�ѧʽΪ___________________________������֪炙�������Ħ������Ϊ960gmol-1,��������в����ǹ�����ʧ�������ܽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I������250mL0.5mol/L��NaOH��Һ��������������ձ�����������������ƽ����ͷ�ιܺ�_______������ʱ���ӹ۲�̶��ߣ�����_______��������ƫ��������ƫС��������������)
����ʵ�����ü��ȹ����Ȼ�狀��������ƵĻ������ȡ��������Ӧ�Ļ�ѧ����ʽ��_______�����Ƶõ������г����������������壬Ϊ�˵õ������İ��������Լ��飬��������װ�û��Լ��У�����Ҫ����������ѡ������Ӧѡ���װ�ñ����ĸ������еĿո�
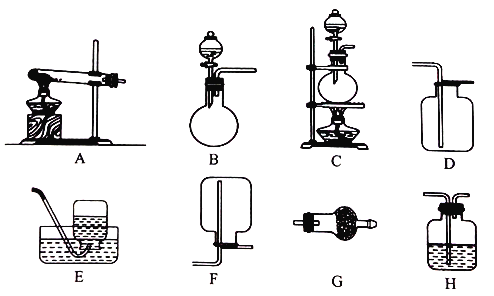
�Լ���a. NaOH��Һ b������ʯ��ˮ c��Ũ���� d������NaHCO3��Һ e����ʯ��
f��Ʒ����Һ g��ʪ��ĺ�ɫʯ����ֽ
��ȡ���� | �������� | ��ȡ����� ����װ�� | �ռ�װ�� | ����װ���� ���õ��Լ� | �����Ƶõ����� �����Լ� |
NH3 | H2O��g�� | _______ | F | e | _______ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����и����е������л��������a.��ͬ�����ʡ�b.ͬϵ�c.ͬ���칹�壬���ж�����֮��Ĺ�ϵ(����ĸ���)��
�ټ���ױ����ұ�____________��
���������2��2����������____________��
��2��������Ͷ���_________��
��1����ϩ�ͻ�����___________________��
��2����д�����и߷��ӻ�����ĵ�����ɵ������ɸ߾���Ľṹ��ʽ��
�� ______________________��
______________________��
�� ______________________��
______________________��
��CH3COOCH��CHCl____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ʯ�ͼ۸����ǣ���úΪԭ���Ʊ�һЩ������Ʒ��ǰ���ֱ����á���ͼ������AΪԭ������������ë�ĺϳ�·�ߡ�

����˵����ȷ���� (����)
A���ϳ�������ë�ķ�Ӧ�������۷�Ӧ
B��A����C�ķ�Ӧ���ڼӳɷ�Ӧ
C��A����D�ķ�Ӧ����ȡ����Ӧ
D����A�Ľṹ��ʽΪCH2===CH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ַ��ӵ����ģ������ͼ��ʾ(ͼ��������֮������߿ɴ���������˫����������)��

��ͬ��ʽ���������ͬ��ԭ�ӣ��Ը����ʵ��ж���ȷ����
A���ٴ��Ļ�ѧ����̼̼˫��
B���ڴ���ԭ�ӿ�������ԭ��
C���÷����е�ԭ�Ӳ����ܾ���ͬһֱ����
D���÷��Ӳ�������״ͬ���칹��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com