
【题目】(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):

请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是____________,
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________。
②上述配离子中含有的化学键类型有:__________________。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为_______;其中铜离子的配位数是_______。
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为__________________
②Fe元素位于周期表的_____区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____;
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______和______(填化学式)。
③根据VSEPR理论预测ED4-离子的空间构型为_________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为____________(写2种)。
【答案】 sp3 前者存在分子间氢键 a、b、c 氯化二乙二胺合铜(Ⅱ) 4 4s24p1 d区 0 N2 【答题空10】CN- (合理即给分) 正四面体 CO2、NCl3、CCl4、CO(任写2个)
【解析】(1)①乙二胺中N原子形成3个σ键,含有1对孤对电子,杂化轨道数目为4,N原子采取sp3杂化;乙二胺分子间存在氢键,含有分子间氢键的沸点较高,所以乙二胺沸点高于Cl-CH2CH2-Cl;故答案为:sp3;前者分子间存在氢键;
②Cu2+离子与N原子之间形成配位键,乙二胺中N原子与H原子之间、N原子与C原子之间形成极性键,碳原子之间形成非极性键,所以存在配位键、极性键、非极性;故答案为:a、b、c;
③已知 中含有的氨基、乙基,铜离子为+2价,则配合物[Cu(en)2]Cl2的系统命名为氯化二乙二胺合铜(II);由图可知铜离子形成4个配位键,铜离子的配位数是4,故答案为:氯化二乙二胺合铜(II);4;
中含有的氨基、乙基,铜离子为+2价,则配合物[Cu(en)2]Cl2的系统命名为氯化二乙二胺合铜(II);由图可知铜离子形成4个配位键,铜离子的配位数是4,故答案为:氯化二乙二胺合铜(II);4;
(2)①Ga是第四横行第十一纵行的元素,所以是第四周期第IIIA族的元素,最外层电子排布式为4s24p1,故答案为:4s24p1;
②Fe原子是26号元素,Fe原子的基态核外电子排布式为:1s22s22p63s23p63d64s2,这些能级的能量大小顺序为:1s<2s<2p<3s<3p<4s<3d,最后排入的是3d电子,因此属于d区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中CO为电中性,则铁的化合价为0价; CO的等电子体必须是双原子分子或离子,且电子总数相等。CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2;如果是阳离子离子或阴离子,原子序数之和减去或加上所带电荷数值=14,所以有CN-,故答案为:d区;0价;N2; CN-;
③根据元素周期表知,E是Cl元素,D是O元素,ED4-是ClO4-离子,中心原子是Cl原子,中心原子结合的原子个数是4,所以σ键电子对数=4,中心原子上的孤电子对数=1/2(a-xb)=1/2(8-4×2)=0,所以价层电子对数=4,根据VSEPR理论预测ED4-离子的空间构型为正四面体型;根据元素周期表知,B、C、D、E分别是C、N、O、Cl是四种元素,分子中每个原子最外层都达到8电子稳定结构的判断公式是:化合价的绝对值+原子最外层电子数=8,分子中每个原子最外层都达到8电子稳定结构,否则就没有达到8电子稳定结构。所以两两形成的化合物且每个原子最外层都达到8电子稳定结构的化合物有:CO2、NCl3、CCl4、CO,故答案为:正四面体;CO2、NCl3、CCl4、CO(任写2个)。


科目:高中化学 来源: 题型:
【题目】现有常温下的六份溶液:①0.01mol/LCH3COOH溶液;②0.01mol/LHCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol/LCH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01mol/LHCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
⑴其中水的电离程度最大的是 (选填序号,下同),水的电离程度相同的是 ;
⑵若将②、③混合后所得溶液pH=7,则消耗溶液的体积:② ③(选填“>”、“<”或“=”);
⑶将六份溶液稀释相同倍数后,溶液的pH:① ②,③ ④,⑤ ⑥(选填“>”、“<”或“=”);
⑷将①、④混合,若有c(CH3COO-)>c(H+),则混合液可能呈 (填序号)
A.酸性 B.碱性 C.中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气通过软管灌入田鼠洞中可用于消灭田鼠,这是利用了Cl2的那些性质
①黄绿色 ②密度比空气大 ③有毒 ④容易液化
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
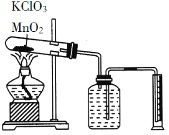
实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279. 7 mL。
⑤准确称量试管和残留物的质量为15. 55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
这三步操作的正确顺序是_________________(请填写步骤代号)。
进行③的实验操作时,若仰视读数,则读取氧气的体积_______(填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是_____mol;实验测得氧气的气体摩尔体积是______(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在5-氨基四唑(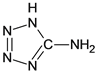 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为__________;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为__________;在1mol 5-氨基四唑中含有的σ键的数目为__________.
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂.
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为__________.
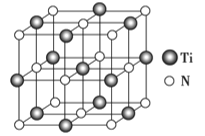
②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化 钛化合物.其结构是用碳原子取代氮化钛晶胞(结构如图示)顶点的氮原子,这种碳氮化钛化合物的化学式为__________.
③[Ti(OH)2(H2O)4]2+中的化学键有__________.
a.σ键 b.π键 c.离子键 d.配位键.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)下列六种生活中常见物质:
①食盐 ②食用油 ③靑霉素 ④鸡蛋 ⑤西红柿 ⑥塑料
按要求用物质序号填空:
作调味剂的是___________;作抗生素的是___________;富含蛋白质的是___________;富含维生素的是___________;富含油脂的是___________;属于合成材料的是___________。
(2)一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+, 有利于人体吸收。
i.在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
ii.服用维生索C,可使食物中的Fe3+还原成Fe2+这句话指出,维生素C在这一反应中作 ____________(填“氧化剂”或“还原剂”)
iii.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸 (HC1)的作用下转化成亚铁盐。此反应的离子方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示取1 mol己烯雌酚进行的四个实验,下列对实验数据的预测与实际情况吻合的是

A. ①中生成7 mol H2O B. ②中生成2 mol CO2
C. ③中最多消耗3 mo1 Br2 D. ④中最多消耗7 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是( )
①下表数据可以计算出 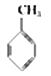 (g)+3H2(g)→
(g)+3H2(g)→ 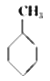 (g)的反应热;
(g)的反应热;
共价键 | C﹣C | C═C | C﹣H | H﹣H |
键能/(kJmol﹣1) | 348 | 610 | 413 | 436 |
②已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1, 则氢气的燃烧热为△H=﹣241.8kJmol﹣1
③由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
④X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
A. ①②③④ B. ③④⑤ C. ④⑤ D. ⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com