
【题目】
(1)下列六种生活中常见物质:
①食盐 ②食用油 ③靑霉素 ④鸡蛋 ⑤西红柿 ⑥塑料
按要求用物质序号填空:
作调味剂的是___________;作抗生素的是___________;富含蛋白质的是___________;富含维生素的是___________;富含油脂的是___________;属于合成材料的是___________。
(2)一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+, 有利于人体吸收。
i.在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
ii.服用维生索C,可使食物中的Fe3+还原成Fe2+这句话指出,维生素C在这一反应中作 ____________(填“氧化剂”或“还原剂”)
iii.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸 (HC1)的作用下转化成亚铁盐。此反应的离子方程式为___________________________________。
【答案】 ① ③ ④ ⑤ ② ⑥ 还原剂 氧化剂 还原剂 Fe+2H+=Fe2++H2↑
【解析】(1)①食盐有咸味,可做调味剂;②食用油富含油脂;③青霉素是抗生素;④鸡蛋富含蛋白质;⑤西红柿富含维生素⑥塑料是人工合成材料,故答案为:①;③;④;⑤;②;⑥;
(2)i.Fe2+→Fe3+的转化时,元素的化合价升高,作还原剂;Fe3+→Fe2+转化时,元素的化合价降低,作氧化剂,故答案为:还原剂;氧化剂;
ii.维生素C,可使食物中的Fe3+还原成Fe2+,Fe元素的化合价降低,作氧化剂,则维生素C具有还原性,作还原剂,故答案为:还原剂;
iii.铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐的离子方程式为:Fe+2H+═Fe2++H2↑,故答案为:Fe+2H+═Fe2++H2↑。


科目:高中化学 来源: 题型:
【题目】当反应条件(如温度、浓度或物质的量等)发生改变时,下列不会引起生成物发生改变的是
A. 钠和氧气 B. 锌和硫酸 C. 氢氧化钠和二氧化碳 D. 氢气和氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):

请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是____________,
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________。
②上述配离子中含有的化学键类型有:__________________。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为_______;其中铜离子的配位数是_______。
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为__________________
②Fe元素位于周期表的_____区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____;
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______和______(填化学式)。
③根据VSEPR理论预测ED4-离子的空间构型为_________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为____________(写2种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】硼和氮元素在化学中有很重要的地位,回答下列问题:
(1)基态硼原子核外电子有________种不同的运动状态,基态氮原子的价层电子排布图为_________。预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2]。(CH3)2NNH2中N原子的杂化方式为_________。
(2)化合物H3BNH3是一种潜在的储氢材料,可利用化合物B3N3H6通过如下反应制得:3CH4+2B3N3H6+6H2O=3CO2+6H3BNH3
①H3BNH3分子中是否存在配位键_______________(填“是”或“否”),B、C、N、O的第一电离能由小到大的顺序为___________________。
②与B3N3H6互为等电子体的分子是_____________(填一个即可),B3N3H6为非极性分子,根据等电子原理写出B3N3H6的结构式____________________________。
(3)“嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:
①SeO3分子的立体构型为_____________。
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 。
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为![]() pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿伏伽德罗常数的值)。
pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿伏伽德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表列出了①~⑥六种元素在元素周期表中的位置.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是 (填写元素符号);
(2)元素①③⑥的氢化物的分子式分别是 ; ; .
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)下表为长式周期表的一部分,其中的编号代表对应的元素。
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | [ | ⑦ | |||||||||||||
⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区元素的是 (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为________________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑦和⑧形成的化合物的电子式为 。
(6)元素⑩的基态原子核外电子排布式是 。
(7)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I 、金属镁性质活泼,能与许多物质反应,某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2燃烧,可能产物为MgO、N2和Mg3N2。通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。己知:NO2气体能被NaOH吸收,Mg3N2极易与水反应。
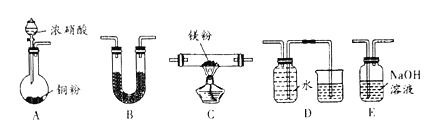
(1)实验中,装置依次连按的顺序为A _________(填字母序号);装置B 的作用是______;
(2)用来检验N2的实验装置为__________(填字母序号);
(3)设计实验证明:产物中存在Mg3N2 ____________;
Ⅱ、工业上以菱镁矿为原料(主要成分为MgCO3,还有SiO2、FeCO3等杂质)制备纳米氧化镁。
(4)根据反应流程要求,先除去FeCO3,采用先酸浸再氧化的方法,其中加入H2O2时,发生反应的离子方程式为__________。
(5)已知:在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,流程后期,当除杂完成后,再加入CO(NH2)2 开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或离子反应方程式表示)___________;___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组中的两种有机物,可能是a.相同的物质、b.同系物、c.同分异构体,请判断它们之间的关系(用字母填空):
①间二甲苯和乙苯____________;
②新戊烷和2,2-二甲基丙烷____________;
③2-甲基丁烷和丁烷_________;
④1-己烯和环己烷___________________。
(2)请写出下列高分子化合物的单体或由单体生成高聚物的结构简式。
① ______________________;
______________________;
② ______________________;
______________________;
③CH3COOCH=CHCl____________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com