
【题目】除去混在碳酸钠粉末中的少量碳酸氢钠,最合理的方法是( )
A. 加热 B. 加入氢氧化钠溶液 C. 加入盐酸 D. 加入CaCl2溶液
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】美国医学家证实了3价铬离子(Cr3+)是构成葡萄糖耐量因子的重要组成部分,能够增强胰岛素的作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。
(1)Cr的外围电子排布图为_______________________________ 。
(2)SO2分子的空间构型为__________,是__________ 分子(填“极性”或“非极性”);SO32-离子中心原子的杂化方式为__________。
(3)SCN的电子式为_________________,它的等电子体中属于分子的有___________。
(4)四种分子:①CH4、②SO3、③H2O、④NH3,键角由大到小的排列顺序是________(填序号)。
(5)NH3分子可以与H+ 结合生成NH4+,这个过程发生改变的是_____
a. 微粒的空间构型 b. N原子的杂化类型 c. H-N-H的键角 d. 微粒的电子数
(6)由碳元素形成的某种单质的片状和层状结构如图1所示,由碳元素形成的某种晶体的晶胞结构如图2所示,试回答:
①在图1中,碳原子所形成的六元环数、C原子数、C-C键数之比为_____________;
②在图2中,已知阿伏伽德罗常数为NA,晶体密度为ρ g/cm3,则该晶体的棱长为
________________pm(只列式,不计算)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不正确的是
A. 分液漏斗使用前需要先检查是否漏液
B. 实验中剩余的钠不能再放回原试剂瓶
C. 做焰色反应时,铂丝应用盐酸洗净并灼烧至无色
D. 蒸馏烧瓶加热时需要垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气通过软管灌入田鼠洞中可用于消灭田鼠,这是利用了Cl2的那些性质
①黄绿色 ②密度比空气大 ③有毒 ④容易液化
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 X、Y、Z均为短周期元素。已知X元素的原子核内无中子,Y元素的原子核外最外层电子数是其次外层电子数的2倍,Z元素是地壳中含量最丰富的元素。有下列含该三种元素的化学式:①X2Y2Z2 ②X2YZ3 ③X2YZ2 ④X2Y2Z4 ⑤X3YZ4 ⑥XYZ3,其中可能存在对应物质的是
A. 只有② B. 只有②④ C. 只有②⑤⑥ D. 只有①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
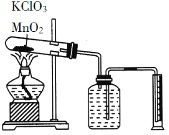
实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279. 7 mL。
⑤准确称量试管和残留物的质量为15. 55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
这三步操作的正确顺序是_________________(请填写步骤代号)。
进行③的实验操作时,若仰视读数,则读取氧气的体积_______(填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是_____mol;实验测得氧气的气体摩尔体积是______(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)下列六种生活中常见物质:
①食盐 ②食用油 ③靑霉素 ④鸡蛋 ⑤西红柿 ⑥塑料
按要求用物质序号填空:
作调味剂的是___________;作抗生素的是___________;富含蛋白质的是___________;富含维生素的是___________;富含油脂的是___________;属于合成材料的是___________。
(2)一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+, 有利于人体吸收。
i.在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
ii.服用维生索C,可使食物中的Fe3+还原成Fe2+这句话指出,维生素C在这一反应中作 ____________(填“氧化剂”或“还原剂”)
iii.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸 (HC1)的作用下转化成亚铁盐。此反应的离子方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将盛有N2和NO2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体的体积缩小为原体积的三分之二,则原混合气体中氮气和二氧化氮的体积比是( )
A. 1:3 B. 1 :2 C. 1:1 D. 3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com