
【题目】水合肼(N2H4·H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:
CO(NH2)2+2NaOH+NaC1O==N2H4·H2O+Na2CO3+NaCl。

实验1:制备NaClO溶液。(已知:3NaClO![]() 2NaCl+NaClO3)
2NaCl+NaClO3)
(1)图甲装置I中烧瓶内发生反应的化学方程式为_______________________。
(2)用NaOH固体配制溶质质量分数为30%NaOH溶液时,所需玻璃仪器除量筒外还有________________。(填标号)
a.烧杯 b.容量瓶 c.玻璃棒 d.烧瓶
(3)图甲装置Ⅱ中用冰水浴控制温度的目的是_________________。
实验2:制取水合肼。
(4)图乙中若分液漏斗滴液速度过快,部分N2H4·H2O会参与A中反应并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式:________________________。充分反应后,蒸馏A中溶液即可得到水合肼的粗产品。
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15 mol·L-1的碘的标准溶液滴定。(已知:N2H4·H2O+2I2==N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在________(填“酸式”或“碱式”)滴定管。
②下列能导致馏分中水合肼的含量测定结果偏高的是_________。(填标号)
a.锥形瓶清洗干净后未干燥
b.滴定前,滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后俯视
d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为_______________________。
【答案】 MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O ac 防止NaClO分解,影响水合肼的产率 N2H4·H2O+2NaClO=N2↑+3H2O+2NaCl 酸式 d 25%
MnCl2+Cl2↑+2H2O ac 防止NaClO分解,影响水合肼的产率 N2H4·H2O+2NaClO=N2↑+3H2O+2NaCl 酸式 d 25%
【解析】(1)二氧化锰与浓盐酸反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-![]() Mn2+Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2+Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2+Cl2↑+2H2O;
Mn2+Cl2↑+2H2O;
(2)配制30%NaOH溶液时,用天平称量质量,在烧杯中加水溶解,并用玻璃棒搅拌,需要玻璃仪器有:烧杯、玻璃棒,故答案为:ac;
(3)由于温度升高时,次氯酸钠容易发生自身的氧化还原反应生成氯酸钠和氯化钠,所以步骤1温度需要在30℃以下,其主要目的是防止NaClO(歧化)分解为氯酸钠和氯化钠,故答案为:防止NaClO(歧化)分解,影响水合肼的产率;
(4)N2H4H2O具有强还原性,容易被过量的NaClO氧化,会发生反应:N2H4H2O+2NaClO=N2↑+3H2O+2NaCl,故答案为:N2H4H2O+2NaClO=N2↑+3H2O+2NaCl;
(5)①碘的标准溶液显酸性,应该盛放在酸式滴定管中,故答案为:酸式;
②a.锥形瓶清洗干净后未干燥,对实验结果无影响,错误;b.滴定前,滴定管内无气泡,滴定后有气泡,导致标准液的体积偏小,则结果偏低,错误;c.读数时,滴定前平视,滴定后俯视,导致滴定后读数偏小,使得标准液的体积偏小,则结果偏低,错误;d.盛标准液的滴定管水洗后,直接装标准液,使得标准液的浓度偏小,造成滴定后标准液的体积偏大,则结果偏高,正确;故选d;
③设馏分中水合肼(N2H4H2O)的质量分数为a,则:
N2H4H2O+2I2=N2↑+4HI+H2O
50g 2mol
0.3000g×a 0.020L×0.15mol/L
所以50g:0.3000g×a=2mol:0.020L×0.15mol/L,解得:a=25%,故答案为:25%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
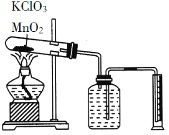
实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279. 7 mL。
⑤准确称量试管和残留物的质量为15. 55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
这三步操作的正确顺序是_________________(请填写步骤代号)。
进行③的实验操作时,若仰视读数,则读取氧气的体积_______(填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是_____mol;实验测得氧气的气体摩尔体积是______(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示取1 mol己烯雌酚进行的四个实验,下列对实验数据的预测与实际情况吻合的是

A. ①中生成7 mol H2O B. ②中生成2 mol CO2
C. ③中最多消耗3 mo1 Br2 D. ④中最多消耗7 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为________________________。放电一段时间后,负极附近溶液的pH________(填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为________________________。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。_______

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
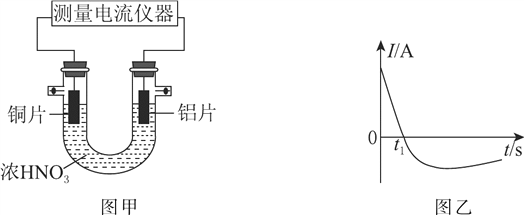
t1s前,原电池的负极是铝片,正极的电极反应式为____________,溶液中的H+向________(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将盛有N2和NO2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体的体积缩小为原体积的三分之二,则原混合气体中氮气和二氧化氮的体积比是( )
A. 1:3 B. 1 :2 C. 1:1 D. 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是2004年批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下 提供质子(H+)和电子。电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为:2CH3OH+3O2=2CO2+4H2O。下列说法中不正确的是
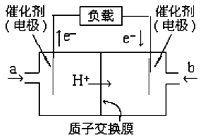
A. 左边的电极为电池的负极,a处通入的是甲醇
B. 每消耗3.2克氧气转移的电子数为0.4mol
C. 电池负极的反应式为:CH3OH + H2O — 6e—==CO2+ 6H+
D. 电池的正极反应式为:O2+2H2O+4e—==4OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是( )
①下表数据可以计算出 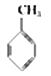 (g)+3H2(g)→
(g)+3H2(g)→ 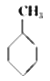 (g)的反应热;
(g)的反应热;
共价键 | C﹣C | C═C | C﹣H | H﹣H |
键能/(kJmol﹣1) | 348 | 610 | 413 | 436 |
②已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1, 则氢气的燃烧热为△H=﹣241.8kJmol﹣1
③由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
④X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
A. ①②③④ B. ③④⑤ C. ④⑤ D. ⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都正确的是( )
选项 | 反应类型 | 反应条件 |
A | 加成反应、取代反应、消去反应 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去反应、加成反应、取代反应 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
C | 氧化反应、取代反应、消去反应 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是( )
A. 由乙醇制备乙烯;由乙烯制备乙醇
B. 由苯制备溴苯;由甲苯制备TNT
C. 由乙醛制备乙酸;由乙醛制备乙醇
D. 由油酸甘油酯制备硬脂酸甘油酯;由硬脂酸甘油酯制备硬脂酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com