
| m |
| M |
| m |
| M |
. |
| M |
| m总 |
| n总 |


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学变化都伴随着能量变化 |
| B、伴有能量变化的物质变化都是化学变化 |
| C、在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定相等 |
| D、在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
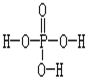 磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )
磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )| A、Na5P3O1212mol |
| B、Na3H2P3O10 9mol |
| C、Na5P3O109mol |
| D、Na2H3P3O10 12mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、乙酸钠溶液显碱性原因:CH3COO-+H2O=CH3COOH+OH- |
| C、氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O |
| D、漂白粉放置在空气中变质:ClO-+CO2+H2O=HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com