
 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.| 10.8g |
| 108g/mol |
| 10.8g |
| 108g/mol |
| ||
| 20% |


科目:高中化学 来源: 题型:
| A、电池正极反应式为2MnO2+2H2O+2e-═2MnO(OH)+2OH- |
| B、电池工作时,电子通过外电路从正极流向负极 |
| C、当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 |
| D、该电池反应中二氧化锰起催化作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠长期暴露在空气中,表面变暗最终生成白色固体氧化钠 |
| B、钠着火时,我们可以用煤油扑灭 |
| C、金属原子最外层电子越少,其还原性越强 |
| D、铝表面有致密的氧化膜,所以铝在空气中能稳定存在而且应用非常广泛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 4 |
| A、H2和O2 |
| B、HCl和NH3 |
| C、H2和Cl2 |
| D、NO和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol乙烷分子中含有8NA个共价键 |
| B、0.05mol熔融的KHSO4中含有阳离子的数目为0.05 NA |
| C、标准状况下,22.4L甲醇的分子数为NA |
| D、1mol/L的氯化铵溶液含氮原子数为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化钠溶液中滴入硝酸银溶液 |
| B、铁片置于硫酸铜溶液中 |
| C、金属钠在氯气中燃烧 |
| D、二氧化碳通入澄清石灰水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
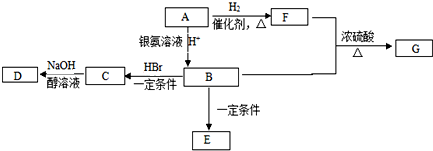
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com