

���� ���̷����������ϣ����������ơ�þ�Ͻ�Ϊ������ȡ��������NiC2O4•2H2O�����ٸ������ղ�������ȡ�����������������ϼ������ܽ����˵õ���Һ�к����������ӡ������ӡ�þ���ӡ������ӣ������������������������Ϊ�����ӣ�����̼������Һ������Һ��PH��ʹ������ȫ�����������˺����Һ�ڼ���NH4F���������Ӻ�þ���ӣ����˵õ���Һ���������ӵ���Һ������Һ�м���������ɲ�����������Ũ���ᾧ��������ΪĿ�����NiC2O4•2H2O��
��1������ʱ�ò���������������
��2����������������������Ϊ�����ӣ����ݵ���غ��ԭ���غ㣬����Na2CO3��Һ��pH��4.0〜4.5���ٽ�������ˮ���γ��������������������ơ�����þ������ˮ��
��3����������NiC2O4•2H2O�����ȿ����и�����ˮ������NiC2O4��NiC2O4�ٷ���������ԭ��Ӧ��Ni��+2�����ߵ�+3�ۣ���C��+3�۽��͵�+2�ۣ�����Ҫ�����ɻ�����壬����һ����ΪCO2������Ni2O3��CO��CO2�������û��ϼ����������ƽ��
��4��Cl��+1�۽��͵�-1�ۣ�Ni��+2�����ߵ�+3�ۣ����û��ϼ�������ȿ���ƽClO-��Ni��OH��2��Cl-��Ni2O3��ϵ����������Hԭ���غ���ƽˮ��ϵ������������Oԭ�Ӽ����ƽ�Ƿ���ȷ�����ݻ�ѧ����ʽ��Ԫ���غ����õ���
��5�����ݣ�4���ļ�������ԭ���غ����д����ѧʽ��
��� �⣺��1������ʱ�ò����������������ʴ�Ϊ��������
��2����˫��ˮ��Ŀ���ǰ�Fe2+��������Fe3+������̼������Һ���������к����H+������pH���ٽ�������ˮ�������ȫ���ټ���NH4F��Ŀ���dz�ȥ�����ӡ�þ���ӣ�ʹ���Ӳ���ʱ���ɲ�����������
�ʴ�Ϊ������pH���ٽ�������ˮ�������ȫ����ȥCa2+��Mg2+��
��3����������NiC2O4•2H2O�����ȿ����и�����ˮ������NiC2O4��NiC2O4�ٷ���������ԭ��Ӧ��Ni��+2�����ߵ�+3�ۣ���C��+3�۽��͵�+2�ۣ�����Ҫ�����ɻ�����壬����һ����ΪCO2������Ni2O3��CO��CO2�������û��ϼ�������ȣ�Ni������2����3-2����C������1����4-3����C�����ͣ�3����3-2������ƽ����ʽΪ��2NiC2O4$\frac{\underline{\;����\;}}{\;}$Ni2O3+3CO��+CO2����
�ʴ�Ϊ��2NiC2O4$\frac{\underline{\;����\;}}{\;}$Ni2O3+3CO��+CO2����
��4��Cl��+1�۽��͵�-1�ۣ�Ni��+2�����ߵ�+3�ۣ����û��ϼ�������ȿ���ƽClO-��Ni��OH��2��Cl-��Ni2O3��ϵ����������Hԭ���غ���ƽˮ��ϵ������������Oԭ�Ӽ����ƽ�Ƿ���ȷ���õ����ӷ���ʽΪ��ClO-+2Ni��OH��2�TCl-+Ni2O3+2H2O��
ClO-+2Ni��OH��2�TCl-+Ni2O3+2H2O
1 2
n��ClO-�� a mol
��n��ClO-��=0.5 a mol
Cl2+2OH-�TClO-+Cl-+H2O
0.8n��Cl2�� 0.5 a mol
��n��Cl2��=0.625 a mol
���е��ʱ��2Cl--2e-�TCl2��
2 1
n��e-�� 0.625 a mol
��n��e-��=1.25a mol��
�ʴ𰸣�ClO-+2Ni��OH��2�TCl-+Ni2O3+2H2O��1.25a mol��
��5��0.2 molˮ������Ϊ3.6g����m��Ni2O3��=20.2 g-3.6g=16.6g��n��Ni2O3��=0.1mol������n��Ni2O3����n��H2O��=0.1mol��0.2 mol=1��2��������ԭ���غ�д�ɽᾧˮ�������ʽ����1mol�������к���0.5 mol�ᾧˮ������NiOOH•$\frac{1}{2}$H2O�����ϳɣ�2NiOOH•H2O��
�ʴ�Ϊ��NiOOH•$\frac{1}{2}$H2O ��2NiOOH•H2O��
���� ���⿼�������̷����ƶϣ�ʵ���������ķ����жϣ���ѧ����ʽ����͵��ԭ������Ӧ�ã���Ŀ�ۺ��Խϴ���Ŀ�ѶȽϴ�


 Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4��Ħ��������98g | |
| B�� | 1molO2��������32g | |
| C�� | ����Ħ������������ԭ�ӵ����ԭ������ | |
| D�� | 1molNa+��������23g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
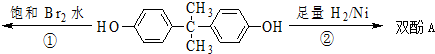
| A�� | ˫��A�ķ���ʽ��C15H16O2 | |
| B�� | ˫��A�ĺ˴Ź���������ʾ��ԭ����֮����1��2��2��3 | |
| C�� | ��Ӧ���У�1 mol˫��A�������4mol Br2 | |
| D�� | ��Ӧ�ڵIJ����������ֹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.92g | B�� | 1.68g | C�� | 2.12g | D�� | 2.55g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | ||
| C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ��屽ʱ����������ˮ��ϣ������� | |
| B�� | ��ȥ�����л��еĶ�����̼ʱ������ͨ���ռ���Һ��Ũ���� | |
| C�� | �����Ը��������Һ�еμӼ��α����������Ϻ�ɫ��ȥ | |
| D�� | �ڱ���ͭ�����Ʊ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
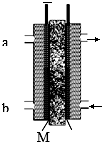 �״���ȼ�ϵ�صij���ԭ�ϣ��������ڵ�K2CO3Ϊ����ʣ��Լ״�Ϊȼ�ϣ��Կ���Ϊ���������Ծ��д����ú͵������ܵ�ϡ����������Ϊ�缫��ͼ�Ǽ״�ȼ�ϵ��ģ�ͣ��Իش��������⣺
�״���ȼ�ϵ�صij���ԭ�ϣ��������ڵ�K2CO3Ϊ����ʣ��Լ״�Ϊȼ�ϣ��Կ���Ϊ���������Ծ��д����ú͵������ܵ�ϡ����������Ϊ�缫��ͼ�Ǽ״�ȼ�ϵ��ģ�ͣ��Իش��������⣺�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com