
【题目】实现下列转化,必须加入氧化剂或还原剂的是( )
A. NO2→HNO3+NO B. ![]() →NH3
→NH3
C. NH3→NO D. P2O5→H3PO4
【答案】C
【解析】
在NO2→HNO3+NO的转化中,化合价变化的均是N元素,二氧化氮本身即是氧化剂又是还原剂;NH4+→NH3的转化中没有元素化合价的变化,属于非氧化还原反应;NH3→NO的转化中,氮元素化合价升高,NH3发生氧化反应;P2O5→H3PO4的转化中没有元素化合价的变化,属于非氧化还原反应。
在NO2→HNO3+NO的转化中,化合价变化的均是N元素,二氧化氮本身既是氧化剂又是还原剂,无需加入氧化剂或还原剂,故不选A;NH4+→NH3的转化中没有元素化合价的变化,属于非氧化还原反应,无需加入氧化剂或还原剂,故不选B;NH3→NO的转化中,氮元素化合价升高,NH3发生氧化反应,需加入氧化剂来实现,故选C;P2O5→H3PO4的转化中没有元素化合价的变化,属于非氧化还原反应,无需加入氧化剂或还原剂,故不选D。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3、K2SO4、KAl(SO4)2三种物质组成的混合溶液中,K+的浓度为0.25mol/L,加入等体积0.20mol/L的KOH溶液,使生成的白色沉淀恰好溶解,那么原溶液中SO42-的浓度是( )
A. 0.20mol/L B. 0.25mol/L C. 0.225mol/L D. 0.45mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,14g有N2与CO组成的混合气体含有的原子数目为NA个
B.0.5molO3与11.2LO2所含的分子数一定相等
C.标准状况下,22.4L四氯化碳的分子数为NA
D.等物质的量的CO和CH4中碳原子数均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列俗名和化学式配对错误的是 ( )
A. 重晶石BaSO4 B. 熟石膏CaSO42H2O
C. 胆矾CuSO4 5H2O D. 漂粉精的有效成份Ca(ClO)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
Ⅰ.甲烷自热重整是一种先进的制氢方法,其反应方程式为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)阅读下图,计算上述反应的反应热ΔH=________kJ·mol-1。

Ⅱ.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为________________________________________________________________________。
(3)以CH4、O2为原料,100mL0.15mol·L-1NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为________________________,各离子浓度由大到小的顺序为________________________________________________________________________。
Ⅲ.利用I2O5消除CO污染的反应为5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
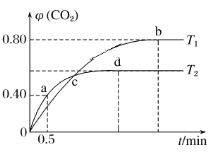
(4)T2时,0~0.5min内的反应速率v(CO)=________________。
(5)T1时化学平衡常数K=________。
(6)下列说法不正确的是________(填标号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。(已知Co2O3的氧化性>Cl2的氧化性)。从废料中回收氧化钴(CoO)的工艺流程如下:
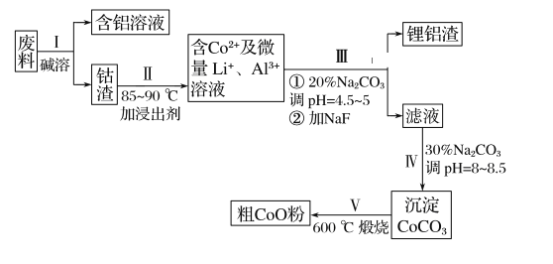
(1)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为__________。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出含钴物质的反应化学方程式为(产物中只有一种酸根)__________________________________。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因:___________________________________________________________。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式:__________________________________。
(4)碳酸钠溶液在过程Ⅲ和Ⅳ中所起作用有所不同,请写出在过程Ⅳ中起的作用是_____。
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是________(填标号)。
A.c(Na+)=2c(CO![]() ) B.c(Na+)>c(CO
) B.c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )
)
C.c(OH-)>c(HCO![]() )>c(H+) D.c(OH-)-c(H+)=c(HCO
)>c(H+) D.c(OH-)-c(H+)=c(HCO![]() )+2c(H2CO3)
)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为浓硫酸与铜反应及其产物检验的实验装置
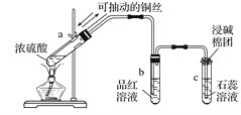
回答下列问题:
(1)指出试管a、b、c中产生的实验现象:
①a中________________________________;
②b中________________________________;
③c中________________________________。
(2)将a试管中的溶液慢慢倒入水中,发生的变化是________________________________。
(3)写出浓硫酸与铜反应的化学方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种盐A和KOH反应,生成有刺激性气味的气体B,B经过一系列氧化再溶于水可得到酸C,B和C反应又可以生成A,则A是 ( )
A. NH4Cl B. (NH4)2SO4 C. NH4NO3 D. (NH4)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
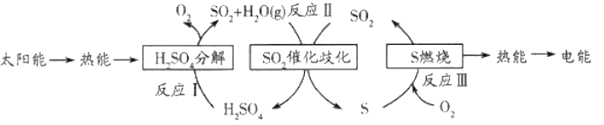
请回答下列问题:
(1)工业生产H2SO4时最后一步反应的化学方程式是_______________________。
(2)反应Ⅰ的化学方程式是_________________。其中氧化产物与还原产物的物质的量之比是________________________。
(3)反应Ⅱ为歧化反应,其中硫元素的化合价是由____________到________________。
(4)反应Ⅲ中硫在氧气中燃烧现象是________________________________。检验生成的二氧化硫的方法是_________________________________________________。观察到的现象是_______________________________。
(5)上述过程中有__________种形式的能量转化,此过程中可能造成一种环境问题是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com