
【题目】向100 mLNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入2.0 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。
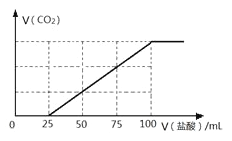
回答下列问题:
(1)原NaOH溶液的物质的量浓度为______ mol/L;
(2)题中通入CO2后所得溶液的溶质成分为______将所得溶质在低温低压条件下蒸干,所得固体物质(不带结晶水)的质量为_______ g。
【答案】2.0Na2CO3和NaHCO313.7 g
【解析】【试题分析】
向100 mLNaOH溶液中通入一定量CO2,充分反应后,所得溶液溶质可能为NaOH和Na2CO3、Na2CO3、Na2CO3和NaHCO3、NaHCO3四种情况,再向所得溶液中逐滴加入2.0 mol/L的盐酸,可能发生的反应为:①NaOH+HCl=NaCl +H2O、②Na2CO3+HCl=NaCl+NaHCO3、③NaHCO3+HCl=NaCl+CO2↑+H2O,结合着可能发生的反应,再根据产生CO2的体积与所加盐酸体积之间关系图,可得通入CO2之后溶质为Na2CO3和NaHCO3,滴加稀盐酸100ml之后溶质为NaCl。
(1)根据题意,NaOH最终转化为NaCl,由原子守恒可得:n(NaOH)= n(NaCl) =n(HCl),又因为100mLNaOH溶液对应100mL盐酸溶液, 所以c(NaOH)= c(HCl)=2.0 mol/L。
(2)由图像可得:滴入25mL稀盐酸后开始发生反应③产生CO2,NaHCO3共消耗了75mL稀盐酸,所以NaOH溶液中通入一定量CO2,充分反应后,所得溶液溶质为Na2CO3和NaHCO3。由图像可得:与Na2CO3反应的盐酸为0.025L×2.0 mol/L=0.05mol,所以Na2CO3为0.05mol,转化为NaHCO3为0.05mol,所以通CO2后生成的NaHCO3消耗的盐酸为0.05L×2.0 mol/L=0.1mol,所以混合物质量为:106g/mol×0.05mol+84g/mol×0.1mol =13.7g。


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
【题目】海藻中含丰富的、以离子形式存在的碘元素。如图是实验室从海藻里提取碘的流程的一部分下列判断正确的是( )
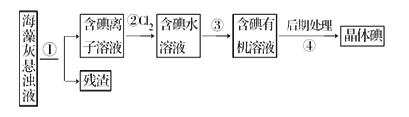
A. 可用淀粉溶液检验步骤②的反应是否进行完全 B. 步骤③中加入的有机溶剂是乙醇
C. 步骤④的操作是过滤 D. 步骤①、③的操作分别是过滤、萃取分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10mL刻度处,现把管内液体全部流下排出,用量筒接收,所得溶液的体积( )
A. 不能确定 B. 为40mL C. 为10mL D. 大于为40mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.非自发反应在任何条件下都不能实现
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.凡是放热反应都是自发的,吸热反应都是非自发的
D.熵增加且放热的反应一定是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的是( )
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混合物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘______。
(2)除去食盐溶液中的水______。
(3)淡化海水______。
(4)KCl中含有KClO3 ______。
II.根据以下装置图,回答下列问题:
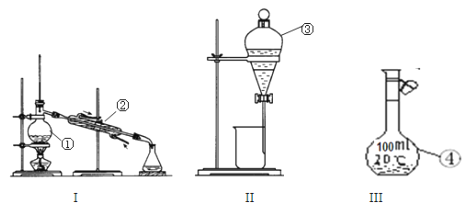
写出仪器名称②______③______;仪器①~④中,使用时必须检查是否漏水的有______(填序号)。
III.某课外活动小组设计下列实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
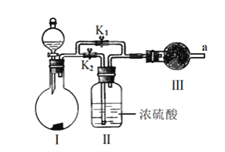
(1)过氧化钠与水反应的化学方程式是______。
(2)装置I是制备纯净的______(填化学式)。则装置I中最适宜的试剂组合是__(填字母) 。
a. 稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2,关闭K1,观察到预期现象后,打开K1,再关闭K2。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是______;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的稀硫酸与足量的铝粉反应时,为了减缓反应速率,且不影响生成氢气的总量,应向稀硫酸中加入适量的( )
A.CH3COOK(固体) B.CH3COOH C.KCl(固体) D.KOH(固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在接触法制硫酸的生产中,SO2转化成SO3转化率的大小直接决定生产效率。某研究小组用下图装置模拟生产过程中测定SO2转化成SO3的转化率。已知SO3的熔点是16.8℃,沸点是44.8℃。装置Ⅰ中所涉及反应的化学方程式为: 。
(1)Ⅱ中的试剂是 ,仪器Ⅵ的名称为 。装置Ⅲ发生反应的化学方程式是 。
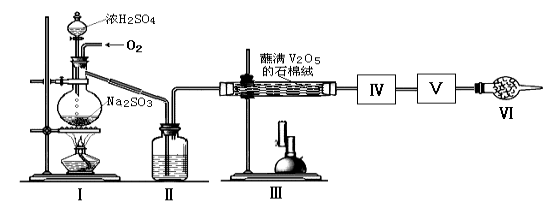
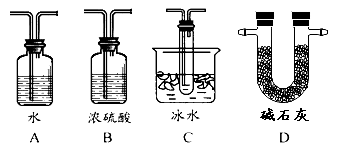
(2)根据实验需要,应该在Ⅳ、Ⅴ处连接合适的装置。请从下图A~D装置中选择最适合装置并将序号填入下面的空格中,Ⅳ、Ⅴ处连接的装置分别是 、 。
(3)为了提高SO2的转化率,实验时在:①滴加浓硫酸;②加热催化剂的步骤中,应采取的操作是先后顺序_____________(填编号)。
(4)实验结束后,如果把收集SO3的试管敞口露置于空气中,能够看到管口有大量的白雾,产生此现象的原因是 。
(5)用18.9gNa2SO3粉末与足量较浓的硫酸进行此实验,当反应结束时,继续通入O2一段时间后测得装置Ⅴ增重了7.2g,则实验测得SO2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定的:①气体分子的直径 ②气体物质的量的多少 ③气体分子间的平均距离 ④气体分子的相对分子质量( )
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com