
【题目】把一块镁铝合金投入到1mol/L盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图A所示。下列说法中不正确的是( )

A.a的取值范围为0≤a<50
B.![]() 的最大值为2.5
的最大值为2.5
C.若将关系图改为B图时,则a的取值范围为80<a<90
D.若将关系图改为C图时,则a的取值范围为75<a<90
【答案】C
【解析】
根据图可知,0→a:H++OH-=H2O、a→80:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,最后80→90:是Al(OH)3的溶解过程,Al(OH)3+OH-=AlO2-+2H2O,从横坐标80mL到90mL这段可以求出n(NaOH)=1mol/L![]() 0.01L=0.01mol,根据反应可知,n[Al(OH)3]=0.01mol,则n(Al)=n[Al(OH)3]=0.01mol,所以Al3+消耗的NaOH溶液的体积为(0.01mol×3)÷1mol/L=0.03L=30mL,据此进行解答。
0.01L=0.01mol,根据反应可知,n[Al(OH)3]=0.01mol,则n(Al)=n[Al(OH)3]=0.01mol,所以Al3+消耗的NaOH溶液的体积为(0.01mol×3)÷1mol/L=0.03L=30mL,据此进行解答。
A.假设合金完全溶解在盐酸中没有H+剩余,则a=0;假设溶液中没有Mg2+,仅有Al3+,则a取最大值,Al3+消耗的NaOH溶液的体积为30mL,a=(80-30)mL=50mL,因是镁铝合金参与反应,则a的取值范围为0≤a<50,A项正确;
B.由上述分析可知n(Al3+)=0.01mol,第四阶段无反应,沉淀全为Mg(OH)2,若a=0,n(Mg2+)取得最大值,第一阶段,和Al3+反应的NaOH为30mL,所以此时和Mg2+反应的NaOH为(80-30)mL=50mL,则此时消耗的氢氧化钠的物质的量为1mol/L![]() 0.05L=0.05mol,故n(Mg2+)max=
0.05L=0.05mol,故n(Mg2+)max=![]()
![]() 0.05mol=0.025mol,所以
0.05mol=0.025mol,所以![]() 的最大值为
的最大值为![]() =2.5,B项正确;
=2.5,B项正确;
C. 若将关系图改为B图时,同样的原理可知,假设溶液中没有Mg2+,仅有Al3+,则此时a取最大值,n(Al3+)=![]() ,则n[Al(OH)3]=n(Al3+)=
,则n[Al(OH)3]=n(Al3+)=![]() ,故此阶段消耗的氢氧化钠的体积为
,故此阶段消耗的氢氧化钠的体积为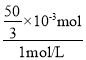 =
=![]() =
=![]() mL,则amax=(80+
mL,则amax=(80+![]() ) mL
) mL![]() 96.7mL,故a的取值范围为80<a<96.7,C项错误;
96.7mL,故a的取值范围为80<a<96.7,C项错误;
D. 若将关系图改为C图时,同样的原理可知,假设溶液中没有Mg2+,仅有Al3+,a取最小值,沉淀0.1mol铝元素需要0.3mol NaOH,溶解该沉淀则需要0.1mol NaOH,则(a-30)mL=3(90-a)mL,解得a=75,故a的取值范围为75<a<90,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B 的转化率变大;当减小压强时,混合体系中 C 的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B 的转化率变大;当减小压强时,混合体系中 C 的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A 的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入 B(体积不变),则 B 的转化率_________。
(4)若 B 是有色物质,A、C 均无色,则加入 C(体积不变)时混合物颜色_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾[KAl(SO4)2·12H2O]的过程如图所示。下列说法正确的是( )

A.试剂①可选用NaOH溶液
B.过滤操作中使用的玻璃仪器只有漏斗、烧杯
C.滤液A到沉淀B的反应中有CO2生成
D.最后一步操作是蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用浓盐酸与氯酸钾固体反应制氯气时,发现所得气体颜色偏深,经分析该气体主要含有Cl2和ClO2两种气体,某研究性学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。

Ⅰ.查阅资料:
常温下二氧化氯为黄绿色气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与NaOH溶液反应生成等物质的量的两种盐,其中一种为 NaClO3。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是____________。
(2)装置C、E的作用分别是 _________、_________。
(3)F中ClO2与NaOH 溶液反应的离子方程式为_____________。
Ⅲ.测量与计算:
反应结束后,测得B、C装置分别增重 2.0g和 14 .2g,将D中的液体溶于水,配成2.5 L溶液,取 25.00 mL该溶液,调节试样的pH﹤2.0 ,加入足量的 KI晶体,振荡后,静置片刻;加入指示剂X ,用 0.200mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00 mL 。(己知: 2ClO2+8H++10I-===5I2+2Cl-+4H2O;2Na2S2O3+I2===Na2S4O6 +2NaI )
(4)指示剂X为_____,滴定终点时的现象是_______________。
(5)原装置收集到的ClO2物质的量为___________。
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)![]() zC(g)。平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断错误的是 ( )
zC(g)。平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断错误的是 ( )
A. x+y<z B. 平衡向逆反应方向移动
C. B的转化率降低 D. C的体积分数下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,0.1mol·L-lCH3COOH的电离度(已电离的CH3COOH分子数/原CH3COOH分子总数)约为1%。该温度下,用0.1000mol·L-l氨水滴定10.00 mL0.1000mol·L-lCH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法正确的是

A. M点→N点,水的电离程度逐渐增大
B. 25℃时,CH3COOH 的电离常数约为1.0×10-2
C. N点溶液中,c(CH3COO-) =c(NH4+)=0.05 mol·L-l
D. 当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可以利用废气中的CO2为原料制取甲醇,反应方程式为CO2+3H2![]() CH3OH + H2O,请回答下列问题:
CH3OH + H2O,请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:

写出二氧化碳和氢气制备甲醇的热化学方程式_______________________________。
(2)如果只改变一个条件使上述反应的平衡常数K值变大,则该反应_____________。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(3)其他条件相同,该甲醇合成反应在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同的时间后,CO2的转化率随反应温度的变化如图所示:

①在相同条件下,三种催化剂Ⅰ、Ⅱ、Ⅲ的催化效率由高到低的顺序是____________。
②c点CO2的转化率高于b点,原因是_________________________________。
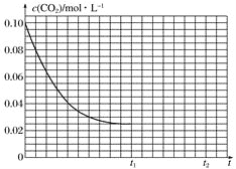
(4)常温常压下若反应的容器容积为2.0L,反应时间为4.0 min,容器里气体密度减少了2.0 g·,在这段时间内CO2平均反应速率为_____________。反应在t1时达到平衡,在这过程中c(CO2)随时间t变化的曲线如下图所示。保持其他条件不变,t1时将容器体积压缩到1 L,请在下图中画出t1后c(CO2)随时间t变化的趋势曲线(假设在t2时达到平衡)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 碳酸钙与足量浓硝酸反应:CaCO3+2H+![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
B. 氢氧化钠溶液与稀醋酸反应:OH-+H+![]() H2O
H2O
C. 氯化铝溶液与过量氨水反应: A13++3OH-=A1(OH)3↓
D. 钠与水反应:Na+2H2O![]() Na++2OH-+H2↑
Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素为周期表前20号元素且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________________________________。
(2)A的气态氢化物溶于水后的电离方程式为________________________________。
(3)B单质在空气中燃烧后的产物的电子式为____________,产物中存在的化学键类型有_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com