
����Ŀ����ҵ�Ͽ������÷����е�CO2Ϊԭ����ȡ�״�����Ӧ����ʽΪCO2+3H2![]() CH3OH + H2O����ش��������⣺
CH3OH + H2O����ش��������⣺
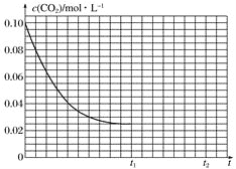
(1)��֪���³�ѹ�����з�Ӧ�������仯����ͼ��ʾ��

д��������̼�������Ʊ��״����Ȼ�ѧ����ʽ_______________________________��
(2)���ֻ�ı�һ������ʹ������Ӧ��ƽ�ⳣ��Kֵ�����÷�Ӧ_____________��
A��һ��������Ӧ�����ƶ� ����������B����ƽ���ƶ�ʱ����Ӧ������������С
C��һ�����淴Ӧ�����ƶ� �������� D����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
(3)����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ���������������������·�Ӧ��ͬ��ʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ��ʾ��

������ͬ�����£����ִ�������������Ĵ�Ч���ɸߵ��͵�˳����____________��
��c��CO2��ת���ʸ���b�㣬ԭ����_________________________________��
(4)���³�ѹ������Ӧ�������ݻ�Ϊ2.0L����Ӧʱ��Ϊ4.0 min�������������ܶȼ�����2.0 g���������ʱ����CO2ƽ����Ӧ����Ϊ_____________����Ӧ��t1ʱ�ﵽƽ�⣬���������c(CO2)��ʱ��t�仯����������ͼ��ʾ�����������������䣬t1ʱ���������ѹ����1 L��������ͼ�л���t1��c(CO2)��ʱ��t�仯���������ߣ�������t2ʱ�ﵽƽ�⣩_________��
���𰸡�CO2(g)��3H2(g)![]() CH3OH(l)��H2O(l) ��H=��50 kJ��mol��1 AD ���������� b��c���δ�ﵽƽ��״̬��c���¶ȸߣ���Ӧ���ʽϿ죬��CO2��ת���ʽϴ� 0.01 mol��L-1��min-1
CH3OH(l)��H2O(l) ��H=��50 kJ��mol��1 AD ���������� b��c���δ�ﵽƽ��״̬��c���¶ȸߣ���Ӧ���ʽϿ죬��CO2��ת���ʽϴ� 0.01 mol��L-1��min-1 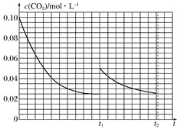
��������
��1������ͼ1�������仯д����Ӧ���Ȼ�ѧ����ʽ��Ȼ����ݸ�˹����д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ��
��2��ƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬�÷�ӦΪ���ȷ�Ӧ��ƽ�ⳣ��������ƽ�����������ƶ���˵���������¶ȣ��ݴ˽��н��
��3������ͼ���ж�����ͬ�¶��£����ֲ�ͬ�Ĵ�����������̼��ת���ʴ�С��ϵ��b��c���δ�ﵽƽ��״̬����c��CO2��ת���ʸ���b�㣬��˶�Ӧ�����������¶ȸߣ���Ӧ���ʽϿ���
��4������������������ܶȼ�С����������������������С�������������������������м��㣻���������Сһ�룬������̼��Ũ������һ����c(CO2) =0.05mol/L�����ù����൱������ѹǿ��CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l) ƽ�������ƶ�������0.025mol/L <c(CO2) <0.05mol/L���ݴ˹��ɻ�ͼ��
CH3OH(l)+H2O(l) ƽ�������ƶ�������0.025mol/L <c(CO2) <0.05mol/L���ݴ˹��ɻ�ͼ��
��1��ͼ1�е��Ȼ�ѧ����ʽΪ��CO��g��+H2O��l��=CO2��g��+H2��g����H=-41kJ/mol����CO��g��+2H2��g��=CH3OH��l����H=-��510-419��kJ/mol=-91KJ/mol�����ݸ�˹������-���ã�������̼�������Ʊ��״����Ȼ�ѧ����ʽ��CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-50KJ/mol����ˣ�������ȷ���ǣ�CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-50KJ/mol��
��2�������Ӧ����ʽCO2+3H2CH3OH+H2O��ƽ�ⳣ��Kֵ�������Ҫ�����¶ȣ�
A�������¶ȣ�ƽ��һ�����������ƶ�����A��ȷ��
B�������¶Ⱥ����淴Ӧ���ʶ���С������Ӧ�����ڴﵽƽ��ǰʼ���ڼ�С����B����
C��ƽ�ⳣ�����Ӧ��Ũ�ȼ�С��������Ũ��������ѧƽ��һ�����������ƶ�����C����
D����ѧƽ�ⳣ�������Ҫ�����¶ȣ������淴Ӧ���ʶ���С����Ϊƽ�����������ƶ������淴Ӧ�����ȼ�С������D��ȷ��
��ˣ�������ȷ���ǣ�AD��
(3)����ͼ��֪������ͬ�¶��£����ֲ�ͬ�Ĵ�����������̼��ת������������������ͬ�����£����ִ������Ĵ�Ч���ɸߵ��͵�˳���������������������������
��c��CO2��ת���ʸ���b�㣬����Ϊb��c���δ�ﵽƽ��״̬��c���¶ȸߣ���Ӧ���ʽϿ����������������������b��c���δ�ﵽƽ��״̬��c���¶ȸߣ���Ӧ���ʽϿ죬��CO2��ת���ʽϴ�
(4)��Ӧ�������ݻ�Ϊ2.0L��������������ܶȼ�С��2.0g/L���������������С��2.0g/L��2.0L=4.0g��
CO2 +3H2 CH3OH +H2O
1mol m 50g
nmol 4g
���Զ�����̼���ٵ����ʵ���Ϊ��n(CO2)=0.08mol�����V(CO2)=��c(CO2)�¦�t= (0.08mol��2L)��4min=0.01mol/(L��min)����ͼ���֪����ӦCO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)����ʼʱc(CO2)=0.10mol/L��ƽ����c(CO2)=0.025mol/L�����������������䣬t1ʱ���������ѹ����1L��������̼��Ũ��Ϊc(CO2)=0.05mol/L��֮��ƽ�����������ƶ���������̼��Ũ�ȼ�С��ֱ��t2ʱ�̴ﵽƽ�⣬t2ʱ�̶�����̼��Ũ��һ������0.025 mol/L����t1ʱ��֮��ͼ����ͼ��
CH3OH(l)+H2O(l)����ʼʱc(CO2)=0.10mol/L��ƽ����c(CO2)=0.025mol/L�����������������䣬t1ʱ���������ѹ����1L��������̼��Ũ��Ϊc(CO2)=0.05mol/L��֮��ƽ�����������ƶ���������̼��Ũ�ȼ�С��ֱ��t2ʱ�̴ﵽƽ�⣬t2ʱ�̶�����̼��Ũ��һ������0.025 mol/L����t1ʱ��֮��ͼ����ͼ��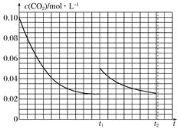 ��
��
�������������������0.01 mol��L-1��min-1 �� ��
��


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У�һ�������ڻ�ѧ���������ת������( )��
A. ���ȷ�ӦB. ������ȼC. �ɱ�����D. ȼ�ű���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��25��ʱ�������ΪVa��pH��a��ijһԪǿ����Һ�����ΪVb��pH��b��ijһԪǿ����Һ��ϣ�ǡ���к͡���ش�
����a��b��12����Va��Vb��________��
����Va��Vb��a��0.5b����a��ȡֵ��Χ��_________________��
II�����ӹ�ҵ�У�����FeCl3��Һ��Ϊӡˢ��·ͭ��ʴ��Һ��ij̽��С�����������·������Һ����Դ���գ�
��ش�

(1)��������FeCl3��Һʴ��ͭ���ķ�Һ�к��еĽ�����������_____________��
(2)������м���H2O2��Һ��Ŀ����________________________________________��
(3)��֪�������������������pH
Cu(OH) 2 | Fe(OH) 2 | Fe(OH) 3 | |
��ʼ����ʱ | 4.7 | 7.0 | 1.9 |
������ȫʱ | 6.7 | 9.0 | 3.2 |
���ݱ��������Ʋ����pH�ķ�Χ��_____________��
(4)��Ҫ��ȥ����MgCl2��Һ�е�FeCl3������Լ�����Լ���_____________��(����ĸ)
A��NaOH B��Mg(OH)2 C��MgCO3 D�� NH3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��þ���Ͻ�Ͷ�뵽1mol/L��������Ͻ���ȫ�ܽ������Һ�����1mol/L NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ����仯�Ĺ�ϵ��ͼA��ʾ������˵���в���ȷ���ǣ� ��

A.a��ȡֵ��ΧΪ0��a��50
B.![]() �����ֵΪ2.5
�����ֵΪ2.5
C.������ϵͼ��ΪBͼʱ����a��ȡֵ��ΧΪ80��a��90
D.������ϵͼ��ΪCͼʱ����a��ȡֵ��ΧΪ75��a��90
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ĵ�������к���ͭ�����Ƚ��������Ϊʵ����Դ�Ļ������ò���Ч��ֹ������Ⱦ��������¹������̣�


(1)��������H2O2��Ŀ����______����pH�������˷�ΧΪ______��
(2)��pH�����м�����Լ������_________��
A��NaOH B��CuO C��NH3��H2O D��Cu2(OH)2CO3
(3)���CuSO4��Һ��ԭ����______����CuSO4��Һ�м���һ������NaCl��Na2SO3���������ɰ�ɫ��CuCl������д���÷�Ӧ�Ļ�ѧ����ʽ________________��
(4)��ȡ���Ʊ���CuCl��Ʒ0.2500g����һ������FeCl3��Һ�У�����Ʒ��ȫ�ܽ���ˮ20 mL����0.1000mol�qL��1��Ce(SO4)2��Һ�ζ��������յ�ʱ����Ce(SO4)2��Һ25.00mL���йصĻ�ѧ��ӦΪFe3++CuCl=Fe2++Cu2++Cl����Ce4++Fe2+=Fe3++Ce3+�������CuCl��Ʒ����������_______________��
(5)��һ���������ü״���CO��Ӧ���ɴ�������CO��Ⱦ�������£���a mol��L��1�Ĵ�����b mol��L��1 Ba(OH)2��Һ�������ϣ���ַ�Ӧ����Һ�д���2c(Ba2��)��c(CH3COO��)����û����Һ�д���ĵ��볣��Ka��_________(�ú�a��b�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL0.5mol/LNaCl��Һ������Cl�����ʵ�����ͬ����Һ��
A.50 mL1mol/LNaCl��ҺB.200mL0.25mol/L AlCl3��Һ
C.100 mL0.5mol/LMgCl2��ҺD.25mL0.5mol/LHCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Z��һ�ֳ����İ뵼����ϣ�����Xͨ������ͼ��ʾ��·���Ʊ�������XΪZ�������YΪ�⻯����ӽṹ��������ƣ��ش��������⣺
![]()
��1������X������ѧ��Ӧ������_________����X�Ʊ�Mg2Z�Ļ�ѧ����ʽΪ_________��
��2����Mg2Z����Y�Ļ�ѧ��Ӧ����ʽΪ_________��Y���ӵĵ���ʽΪ_________��
��3��Z��X�й��ۼ������ͷֱ���_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС���Էϴ�������Ҫ�ɷ�SiO2��ZnO��ZnS��CuS��Ϊԭ�ϣ��Ʊ�п��ͭ�������ξ��塣��Ƶ�ʵ�鷽�����£�

����˵������ȷ���ǣ�������
A. �������������ϡ�������ZnO��ZnS
B. ����١����з����ķ�Ӧ��Ϊ������ԭ��Ӧ
C. ������漰�����ӷ�Ӧ����ΪCuS+H2O2+2H+![]() Cu2++S+2H2O
Cu2++S+2H2O
D. ����ں͢ܣ���������Ũ������ȴ�ᾧ�����˺���ɻ�ȡ�־���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����Ҫ�Ļ����м��壬������ҵ�о����ȵ㡣һ���Ը����̿�(��Ҫ�ɷ�Ϊ���̻����PFeS)Ϊԭ���Ʊ������̵Ĺ����������£�

��֪���١���ϱ��ա���������MnSO4��Fe2O3������FeO��Al2O3��MgO��
�ڽ���������ˮ��Һ�е�ƽ��Ũ����pH�Ĺ�ϵ��ͼ��ʾ(25��)��

�۴�ʵ��������Mn2+��ʼ������pHΪ7.54������Ũ�ȡ�10��5mol��L��1ʱ�����ӳ�����ȫ��
��ش�
(1)��ͳ���մ��������̿�ʱ����������ϱ��ա�������ֱ����H2SO4��������ȱ��Ϊ___________��
(2)��������ʱ��������Ӧ�����ӷ���ʽΪ_________________________________����ʡ�ԡ����������裬��ɵĺ����_________________________________��
(3)���кͳ��ӡ�ʱ�����ɳ�������Ҫ�ɷ�Ϊ______________________(�ѧʽ)��
(4)���������ӡ�ʱ����ʹ��Һ�е�Mg2+��Ca2+������ȫ����ά��c(F��)������___________��(��֪��Ksp(MgF2)=6.4��10��10��Ksp(CaF2)=3.6��10��12)
(5)��̼���ᾧ��ʱ��������Ӧ�����ӷ���ʽΪ______________________��
(6)��ϵ�в�����ָ___________�����ˡ�ϴ�ӡ�����
(7)�ö��Ե缫���MnSO4��Һ���Ʊ�MnO2���������������ĵ缫��ӦʽΪ___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com