
【题目】亚铁氰化钾(K4[Fe(CN)6])又称黄血盐,用于检验Fe3+,也用作实验的防结剂。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
(1)Fe3+的核外电子排布式_________;
(2)与CN-互为等电子体的分子是______,K4[Fe(CN)6]中的作用力除离子键和共价键外,还有_______。含有12mol σ键的K4[Fe(CN)6]的物质的量为_______mol。
(3)黄血盐中C原子的杂化方式为______;C、N、O的第一电离能由大到小的排序为________;
(4)Fe、Na、K的晶体结构如图所示。

①钠的熔点比钾更高,原因是__________;
②Fe原子半径是r cm,阿伏加德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_____g/cm3。
【答案】1s22s22p63s23p63d5 N2 配位键 1 sp N>O>C K和Na的价电子数相同,但Na原子半径小于K原子半径,所以Na金属键更强,熔点更高 ![]()
【解析】
(1)Fe是26号元素,核外有26个电子,失去3个电子得到Fe3+,根据构造原理写出基态Fe3+的核外电子排布式;
(2) CN-有2个原子,价层电子数为10;K4[Fe(CN)6]是离子化合物,其中![]() 含有共价键和配位键,1个
含有共价键和配位键,1个![]() 中含有6个配位键,CN-中含有C≡N,1个C≡N中含有1个σ键、2个π键,即1个
中含有6个配位键,CN-中含有C≡N,1个C≡N中含有1个σ键、2个π键,即1个![]() 中含有12个σ键,据此计算解答;
中含有12个σ键,据此计算解答;
(3)CN中中心原子C的价层电子对数为2,即CN-的VSEPR模型为直线型,采用sp杂化;同一周期元素第一电离能随着原子序数增大而呈增大趋势,但是第IIA族、第VA族元素第一电离能大于其相邻元素;同一周期元素电负性随着原子序数增大而增大;
(4)①金属的金属键越强,熔点越高;
②设晶胞的边长为x,则![]() ,该晶胞中Fe原子数为:8×1/8+1=2,
,该晶胞中Fe原子数为:8×1/8+1=2,![]() ,晶胞密度为:
,晶胞密度为:![]() 计算密度。
计算密度。
(1)Fe原子核外有26个电子,失去3个电子得到Fe3+,基态Fe3+的核外电子排布式:1s22s22p63s23p63d5,故答案为:1s22s22p63s23p63d5;
(2)CN-有2个原子,价层电子数为10,则与CN-互为等电子体的分子为N2;K4[Fe(CN)6]是离子化合物,存在离子键,其中![]() 含有共价键和配位键,即化学键为离子键、配位键和共价键;1个
含有共价键和配位键,即化学键为离子键、配位键和共价键;1个![]() 中含有6个配位键,CN中含有C≡N,1个C≡N中含有1个σ键、2个π键,即1个
中含有6个配位键,CN中含有C≡N,1个C≡N中含有1个σ键、2个π键,即1个![]() 中含有12个σ键,所以含有12mol σ键的K4[Fe(CN)6]的物质的量为1mol,故答案为:N2;配位键;1;
中含有12个σ键,所以含有12mol σ键的K4[Fe(CN)6]的物质的量为1mol,故答案为:N2;配位键;1;
(3)CN中中心原子C的价层电子对数为2,即CN的VSEPR模型为直线型,采用sp杂化;同一周期元素第一电离能随着原子序数增大而呈增大趋势,但是第IIA族、第VA族元素第一电离能大于其相邻元素,所以C.N、O第一电离能大小顺序为N>O>C;故答案为:sp;N>O>C;
(4)①K和Na都为金属晶体,K和Na价电子数相同,但Na原子半径小于K原子半径,所以Na金属键更强,熔点更高,故答案为:K和Na的价电子数相同,但Na原子半径小于K原子半径,所以Na金属键更强,熔点更高;
②设晶胞的边长为x,则![]() ,晶胞体积
,晶胞体积![]() ,该晶胞中Fe原子数为:8×1/8+1=2,
,该晶胞中Fe原子数为:8×1/8+1=2,![]() ,晶胞密度为:
,晶胞密度为: ,故答案为:
,故答案为:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质。一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式__________。
(2)调节pH的目的是___________,pH的调节范围为___________。
(3)生成MnCO3沉淀的离子方程式为___________。
(4)操作A为___________。
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H=" +116.0" kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为___________。
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备__________mol无水Cu(NO3)2。(计算结果精确到小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现极大地推进了现代化的进程,改变了人们的生活方式。关于下图所示原电池的说法 不正确的是 ( )
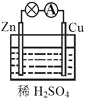
A.该装置将化学能转化为电能
B.反应一段时间后溶液的pH会增大
C.铜片上发生的反应是Cu2+ + 2e-=Cu
D.该装置使氧化反应和还原反应分别在两个不同的区域进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.由水电离出的H+浓度为1×10-9 mol/L的溶液中:Al3+、![]() 、Na+、Cl-
、Na+、Cl-
B.遇酚酞变红的溶液中:![]() 、Na+、
、Na+、![]() 、K+
、K+
C.c(![]() )=1mol/L的溶液中:H+、Fe2+、Cl-、
)=1mol/L的溶液中:H+、Fe2+、Cl-、![]()
D.pH=1的溶液中:![]() 、
、![]() 、K+、Cl-
、K+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出NaHSO4溶液的电离方程式_____; 写出Na2CO3水解的离子方程式_____ ;
(2)25℃时,pH= a的NaOH溶液中, 溶液的C(OH-) =_____ mol/L。
(3)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:(请用相应字母填)
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是______。
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是_____。
③若三者pH相同且体积相等,中和NaOH的能力由大到小的顺序是________。
(4)有下列盐溶液:①MgCl2 ②KNO3 ③KClO ④CH3COONH4 ⑤NaCN⑥Fe2(SO4)3,呈酸性的是________,呈碱性的是________,呈中性的是________(用相应的序号填写)。
(5)请写出明矾(K Al(SO4)212H2O)做净水剂净水时的离子方程式____________;
(6)请写出泡沫灭火器(硫酸铝和碳酸氢钠溶液)灭火时发生反应的离子方程式:____________;
(7)物质的量浓度相同的 氯化铵;②碳酸氢铵;③ 硫酸氢铵;④硫酸铵4种溶液中,c(![]() )由大到小的顺序是_____ (请用相应的序号填写)
)由大到小的顺序是_____ (请用相应的序号填写)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
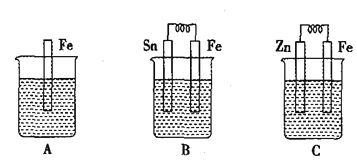
①B中Sn极的电极反应式为__________,Sn极附近溶液的pH_____(填“增大”、“减小”或“不变”)。
②C中总反应离子方程式为_____________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是______(填“a”或“b”)电极,该极的电极反应是_______。
②电池工作一段时间后电解质溶液的pH____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁﹣次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO﹣+H2O═Mg(OH)2+Cl﹣下列有关说法正确的是( )
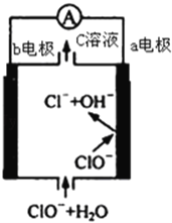
A. 电池工作时,C溶液中的溶质是MgCl2
B. 电池工作时,正极a附近的pH将不断增大
C. 负极反应式:ClO﹣﹣2e﹣+H2O═Cl﹣+2 OH﹣
D. b电极发生还原反应,每转移0.1mol电子,理论上生成0.1mol Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
A.2 s后物质A的转化率为70%
B.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,A和B的转化率都提高
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在相应的条件下,一定能大量共存的是
A.能使pH试纸变蓝的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
B.由水电离产生的 c![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
C.在![]()
![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
D.常温下,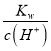
![]() 的溶液中:
的溶液中:![]() 、HCO3-、
、HCO3-、![]() 、
、![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com