
分析 (1)反应生成氯化铜和氯化亚铁;
(2)FeCl3在沸水中可生成胶体,胶体具有丁达尔效应;
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,是由于Fe3+能将I-氧化为I2;当生成1mol碘时,转移2mol电子;向上述溶液中通入二氧化硫气体,I2能和二氧化硫反应生成硫酸和HI;若改加入四氯化碳,则四氯化碳能将I2萃取出来,所使用的主要仪器为分液漏斗.
解答 解:(1)FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,该离子反应为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)将饱和的FeCl3溶液滴入沸水中,继续煮沸至溶液变为红褐色,即可生成红褐色氢氧化铁胶体,则应选C,且胶体具有丁达尔效应,可利用此性质来证明此胶体已经制成,
故答案为:C;丁达尔效应;
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,是由于Fe3+能将I-氧化为I2,离子方程式为:2Fe3++2I-=2Fe2++I2,则生成碘能使淀粉变蓝;此反应中当生成1mol碘时,转移2mol电子,故当生成25.4g的碘即0.1mol碘时,转移0.2mol电子即0.2NA个;向上述溶液中通入二氧化硫气体,I2能和二氧化硫反应生成硫酸和HI,离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+;若改加入四氯化碳,则四氯化碳能将I2萃取出来,故四氯化碳层呈紫红色,萃取时所使用的主要仪器为分液漏斗.故答案为:
2Fe3++2I-=2Fe2++I2,0.2NA,SO2+I2+2H2O=2I-+SO42-+4H+,紫红,分液漏斗.
点评 本题考查知识点较多,涉及离子反应、胶体制备和性质、氧化还原反应、萃取和分液等,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
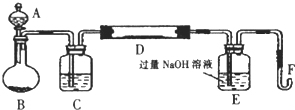
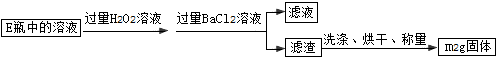
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O溶于水:Na2O+H2O=2Na++2OH- | |
| B. | 向Ca(ClO)2溶液中通入过量CO2:2ClO-+H2O+CO2=2HClO+CO32- | |
| C. | 用FeCl3溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ | |
| D. | 碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属材料都是导体,非金属材料都是绝缘体 | |
| B. | 氢氧化铝可作胃酸的中和剂 | |
| C. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| D. | SO2溶于水能导电,SO2属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
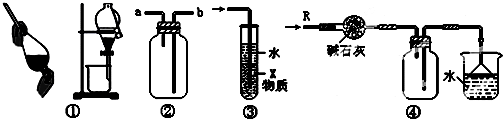
| A. | 装置①可用于分离乙醇和水的混合物 | |
| B. | 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| C. | 装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Ba2+)=c(SO42-) | |
| B. | c(Ba2+)增大,c (SO42-) 减小 | |
| C. | c(Ba2+)≠c SO42-),c(Ba2+)•c(SO42-)=KSP(BaSO4) | |
| D. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)≠KSP(BaSO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
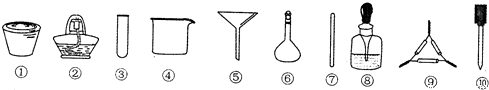
| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 检验滤液中的Fe3+,选用③、⑧和⑩ | |
| C. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| D. | 过滤得到的滤液,选用④、⑤和⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为实验装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com