
【题目】下列化学用语正确的是
A. H2SO3的电离方程式:H2SO3![]() 2H++SO32-
2H++SO32-
B. NaHSO4在水溶液中的电离方程式:NaHSO4= Na++H++SO42-
C. Na2CO3的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. HS-的水解方程式:HS-+ H2O![]() H3O++S2-
H3O++S2-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g)+Q(Q>0)。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,分析正确的是
2SO3(g)+Q(Q>0)。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,分析正确的是

A. 图Ⅰ研究的是t1时刻增大O2的浓度对反应速率的影响
B. 图Ⅱ研究的是t1时刻加入催化剂后对反应速率的影响
C. 图Ⅲ研究的是催化剂对平衡的影响,且甲的催化速率比乙高
D. 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是 ( )
A. 用石墨作电极电解 AlC13 溶液:2Cl- +2H2O![]() Cl2↑+H2↑+2OH
Cl2↑+H2↑+2OH
B. 酸性高锰酸钾溶液与 H2O2 溶液混合:2MnO4 + 3H2O2 + 6H+= 2Mn2++ 4O2↑+6H2O
C. 向硫代硫酸钠溶液中滴加稀硫酸:3S2O32-+2H+=2SO42-+4S↓+H2O
D. 向 Mg(HCO3)2 溶液中加入足量 Ca(OH)2 的溶液:Mg2++2HCO3- +4OH- +2Ca2+=3H2O+2CaCO3↓+ Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置(Ⅰ)为铁镍(Fe﹣Ni)可充电电池:Fe+NiO2![]() Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )

A. 闭合 K 时,X 的电极反应式为:2H++2e═H2↑
B. 给装置(Ⅰ)充电时,OH通过阴离子交换膜,移向 A 电 极
C. 给装置(Ⅰ)充电时,B 极参与反应的物质被氧化
D. 闭合 K 时,A 电极反应式为:NiO2 + 2e +2H+═Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3 作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的 催化剂研究曾被列入国家 863 计划。
(1)催化剂常具有较强的选择性,即专一性。已知:反应 I :4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)
4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I ,测得不同时 间的 NH3 和 O2,的浓度如下表:
时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
c(NH3)/mol·L1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.072 | 0.072 |
c(O2)/mol L1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
则下列有关叙述中正确的是_____。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3) =6v 逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1 时,说明反应已达平衡
D.前 10 分钟内的平均速率 v( NO)=0.088 mol·L-1·min-1
(3)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的 Cu2+。 已知:25℃时,K1(H2S) =1.3×107,K2(H2S) =7.1×1015,Ksp(CuS) =8.5×1045
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则 0.lmol L1 氢硫 酸的 pH≈______(取近似整数)。
②某同学通过近似计算发现 0.lmol L1 氢硫酸与 0.0lmol L1 氢硫酸中的 c(S2)相等,而且 等于_____mol·L1
③已知,某废液接近于中性,若加入适量的氢硫酸,当废液中 c(Cu2+) >_____mol·L1(计算 结果保留两位有效数字),就会产生 CuS 沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用于驱动潜艇的液氨-液氧燃料电池原理示意如图,下列有关该电池说法正确的是

A. 电子由电极A经外电路流向电极B
B. 该电池工作时,每消耗22.4L NH3转移3mol电子
C. 电池工作时,OH-向电极B移动
D. 电极B上发生的电极反应为:O2+ 4H++ 4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
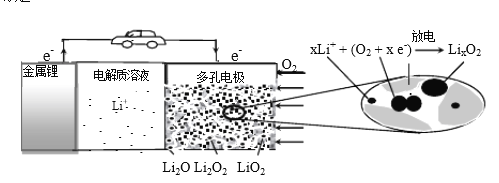
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同情况下测得A(g)+3B(g)![]() 2C(g)+ 2D(s)的下列反应速率,其中反应速率最大的是
2C(g)+ 2D(s)的下列反应速率,其中反应速率最大的是
A. υ(D)=0.01 molL-1s-1 B. υ(C)=0.010 molL-1s-1
C. υ(B)=0.6 molL-1min-1 D. υ(A)=0.2molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知: CO可将部分氮的氧化物还原为N2。
反应I :2CO(g)+2NO(g) ![]() N2(g)+2CO2(g) △H=-746kJ.mol-1
N2(g)+2CO2(g) △H=-746kJ.mol-1
反应II :4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H=-1200kJ.mol-1
N2(g)+4CO2(g) △H=-1200kJ.mol-1
则反应NO2(g)+CO(g) ![]() CO2(g)+NO(g)的△H=______kJ/mol。
CO2(g)+NO(g)的△H=______kJ/mol。
(2)一定条件下,将NO2与CO以体积比1:2置于密闭容器中发生反应II,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.容器中气体密度保持不变
c.混合气体颜色保持不变 d.每消耗2molNO2的同时生成1molN2
(3)温度为T、容积为10L的恒容密闭容器中,充入1molCO和0.5 mol SO2发生反应:2CO(g)+SO2(g)![]() 2CO2(g)+S(g) 实验测得生成的CO2体积分数(φ) 随着时间的变化曲线如图所示:
2CO2(g)+S(g) 实验测得生成的CO2体积分数(φ) 随着时间的变化曲线如图所示:
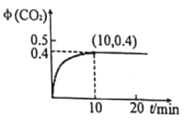
①达到平衡状态时,SO2的转化率为__,该温度下反应的平衡常数K=______。
②其它条件保持不变,再向上述平衡体系中充入SO2(g).CO(g)、S(g)、CO2(g)各0.2mol,此时v(正)___v(逆) (填“>”“<”或“=”)。
(4)SCR法是工业上消除氦氧化物的常用方法,反应原理为4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H<0.在催化剂作用下,NO转化率与温度的关系如图所示:
4N2(g)+6H2O(g) △H<0.在催化剂作用下,NO转化率与温度的关系如图所示:

图中A点处NO的转化率_______(填“可能是”、“一定是 ”或“一定不是”)该温度下的平衡转化率;B点之后,NO转化率降低的原因可能是________。
A.平衡常数变大 B.副反应增多
C.催化剂活性降低 D.反应活化能增大
(5)2SO2(g)+O2(g) ![]() 2SO3(g) △H=-198kJ.mol-l 是制备硫酸的重要反应。在VL恒容密闭容器中充入2molSO2和1molO2,在不同条件下进行反应,反应体系总压强随时间的变化如图所示。a和b平衡时,SO3体积分数较大的是_______; 判断的依据是________。
2SO3(g) △H=-198kJ.mol-l 是制备硫酸的重要反应。在VL恒容密闭容器中充入2molSO2和1molO2,在不同条件下进行反应,反应体系总压强随时间的变化如图所示。a和b平衡时,SO3体积分数较大的是_______; 判断的依据是________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com