
【题目】研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知: CO可将部分氮的氧化物还原为N2。
反应I :2CO(g)+2NO(g) ![]() N2(g)+2CO2(g) △H=-746kJ.mol-1
N2(g)+2CO2(g) △H=-746kJ.mol-1
反应II :4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H=-1200kJ.mol-1
N2(g)+4CO2(g) △H=-1200kJ.mol-1
则反应NO2(g)+CO(g) ![]() CO2(g)+NO(g)的△H=______kJ/mol。
CO2(g)+NO(g)的△H=______kJ/mol。
(2)一定条件下,将NO2与CO以体积比1:2置于密闭容器中发生反应II,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.容器中气体密度保持不变
c.混合气体颜色保持不变 d.每消耗2molNO2的同时生成1molN2
(3)温度为T、容积为10L的恒容密闭容器中,充入1molCO和0.5 mol SO2发生反应:2CO(g)+SO2(g)![]() 2CO2(g)+S(g) 实验测得生成的CO2体积分数(φ) 随着时间的变化曲线如图所示:
2CO2(g)+S(g) 实验测得生成的CO2体积分数(φ) 随着时间的变化曲线如图所示:
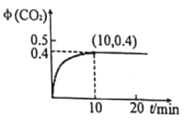
①达到平衡状态时,SO2的转化率为__,该温度下反应的平衡常数K=______。
②其它条件保持不变,再向上述平衡体系中充入SO2(g).CO(g)、S(g)、CO2(g)各0.2mol,此时v(正)___v(逆) (填“>”“<”或“=”)。
(4)SCR法是工业上消除氦氧化物的常用方法,反应原理为4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H<0.在催化剂作用下,NO转化率与温度的关系如图所示:
4N2(g)+6H2O(g) △H<0.在催化剂作用下,NO转化率与温度的关系如图所示:

图中A点处NO的转化率_______(填“可能是”、“一定是 ”或“一定不是”)该温度下的平衡转化率;B点之后,NO转化率降低的原因可能是________。
A.平衡常数变大 B.副反应增多
C.催化剂活性降低 D.反应活化能增大
(5)2SO2(g)+O2(g) ![]() 2SO3(g) △H=-198kJ.mol-l 是制备硫酸的重要反应。在VL恒容密闭容器中充入2molSO2和1molO2,在不同条件下进行反应,反应体系总压强随时间的变化如图所示。a和b平衡时,SO3体积分数较大的是_______; 判断的依据是________。
2SO3(g) △H=-198kJ.mol-l 是制备硫酸的重要反应。在VL恒容密闭容器中充入2molSO2和1molO2,在不同条件下进行反应,反应体系总压强随时间的变化如图所示。a和b平衡时,SO3体积分数较大的是_______; 判断的依据是________。

【答案】 -227 ac 60% 3.375 > 一定不是 BC a b起始压强大于a,说明其温度高于a,而该反应是放热反应,温度升高,平衡逆向移动,SO3体积分数减小
【解析】 (1)已知:反应I:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H=-746kJ.mol-1;反应II:4CO(g)+2NO2(g)
N2(g)+2CO2(g) △H=-746kJ.mol-1;反应II:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) △H=-1200kJ.mol-1。根据盖斯定律,由(II-I)
N2(g)+4CO2(g) △H=-1200kJ.mol-1。根据盖斯定律,由(II-I)![]() 可得反应NO2(g)+CO(g)
可得反应NO2(g)+CO(g)![]() CO2(g)+NO(g),所以其△H=[-1200kJ.mol-1 -(-746kJ.mol-1)]
CO2(g)+NO(g),所以其△H=[-1200kJ.mol-1 -(-746kJ.mol-1)]![]() -227kJ/mol。
-227kJ/mol。
(2)一定条件下,将NO2与CO以体积比1:2置于密闭容器中发生反应II,该反应的正反应是气体分子数减少的反应。a.体系压强保持不变,说明各组分的物质的量保持不变;b.由于气体的质量和体积始终不变,所以容器中气体密度保持不变;c.混合气体颜色保持不变,说明各组分的浓度保持不变;d.每消耗2molNO2的同时生成1molN2,不能说明正反应速率和逆反应速率相等。综上所述,能说明反应达到平衡状态的是ac。
(3)①由图中信息可知,达到平衡状态时,CO2体积分数为0.4,n(CO2)=(1mol+0.5mol)![]() 0.4=0.6mol,则SO2的变化量是0.3mol,其转化率为
0.4=0.6mol,则SO2的变化量是0.3mol,其转化率为![]() 60%。各组分CO、SO2、CO2、S的平衡浓度分别为0.04mol/L、0.02 mol/L、0.06 mol/L、0.03 mol/L,该温度下反应的平衡常数K=
60%。各组分CO、SO2、CO2、S的平衡浓度分别为0.04mol/L、0.02 mol/L、0.06 mol/L、0.03 mol/L,该温度下反应的平衡常数K=![]() =3.375。②其它条件保持不变,再向上述平衡体系中充入SO2(g).CO(g)、S(g)、CO2(g)各0.2mol,此时Qc=
=3.375。②其它条件保持不变,再向上述平衡体系中充入SO2(g).CO(g)、S(g)、CO2(g)各0.2mol,此时Qc=![]() <K,所以反应向正反应方向进行,v(正) >v(逆)。
<K,所以反应向正反应方向进行,v(正) >v(逆)。
(4)由于该反应是放热反应,平衡常数随温度升高而减小,所以其平衡转化率随温度升高而减小,温度越低NO的平衡转化率越大。A点对应的温度低、反应速率较慢,NO的转化率小于B点,所以A点尚未达到平衡状态,故A点NO的转化率一定不是该温度下的平衡转化率;催化剂不变则活化能不变,B点之后,NO转化率降低的原因可能是副反应增多或催化剂活性降低,选BC。
(5) a和b平衡时,SO3体积分数较大的是a,判断的依据是:由图可知,b起始压强大于a,由于容器体积相同、起始投料相同,说明其温度高于a ,而该反应是放热反应,温度升高,平衡逆向移动,SO3体积分数减小。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是
A. H2SO3的电离方程式:H2SO3![]() 2H++SO32-
2H++SO32-
B. NaHSO4在水溶液中的电离方程式:NaHSO4= Na++H++SO42-
C. Na2CO3的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. HS-的水解方程式:HS-+ H2O![]() H3O++S2-
H3O++S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,Ksp[Zn(OH)2]= 1.0×10-18,Ka(HCOOH)=1.0×10-4。该温度下,下列说法错误的是
A. HCOO-的水解常数为1.0×10-10。
B. Zn(OH)2溶于水形成的饱和溶液中,c(Zn2+)>1.0×10-6mol·L-1
C. 向Zn(OH)2悬浊液中加入HCOOH,溶液中c(Zn2+)增大
D. Zn(OH)2(s)+2HCOOH(aq)![]() Zn2+(aq) +2HCOO-(aq)+2H2O(1)的平衡常数K=100
Zn2+(aq) +2HCOO-(aq)+2H2O(1)的平衡常数K=100
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)![]() 2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是


A. 该反应的ΔH<0
B. T1时,该反应的平衡常数为![]()
C. 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2
D. 若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl—,降低对电解的影响,反应原理如下:
Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ΔH1=a kJ·mol-1
2Cu+(aq) ΔH1=a kJ·mol-1
Cl—(aq)+Cu+(aq)![]() CuCl(s) ΔH2=b kJ·mol-1
CuCl(s) ΔH2=b kJ·mol-1
实验测得电解液pH对溶液中残留c(Cl—)的影响如图所示。下列说法正确的是

A. 溶液pH越大,Ksp(CuCl)增大
B. 向电解液中加入稀硫酸,有利于Cl-的去除
C. 反应达到平衡增大c(Cu2+),c(Cl—)减小
D. ![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl—(aq)
Cu2+(aq)+Cl—(aq)![]() CuCl(s)的ΔH=(a+2b) kJ·mol-1
CuCl(s)的ΔH=(a+2b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CaO等,生产工艺流程图如下:

(1)将菱锌矿研磨成粉的目的是___________________________。
(2)写出Fe3+水解的离子方程式_____________________________________________。
(3)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为__________。
沉淀化学式 | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
开始沉淀的pH | 10.4 | 6.4 |
|
|
沉淀完全的pH | 12.4 | 8.0 |
|
|
开始溶解的pH |
| 10.5 |
|
|
Ksp | 5.6×10-12 |
| 6.8×10-6 | 2.8×10-9 |
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是________选填序号。
A、大理石粉 B、石灰乳 C、纯碱溶液 D、氨水
(5)“滤液4”之后的操作依次为______________、______________、过滤、洗涤、干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于__________用代数式表示。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在工业生产、生活中有重要的用途。
(1)硫原子最外层电子轨道表示式为__________。与电子排布式相比,轨道表示式还描述了核外电子运动状态中的______和______。
(2)S、Cl、N三种元素常见的氢化物中,写出属于非电解质的电子式___________。已知PbS与O2在高温时生成铅的氧化物和SO2,化学平衡常数(K)的表达式为:K=![]() 。
。
(3)写出上述反应的化学方程式__________________________。在2L高温密闭容器中加入PbS固体和O2,0~5min内气体质量增加1.6g,则5min内SO2的平均反应速率___________________。
(4)上述反应达到平衡后,说法正确的是_________(选填编号)。
a. 速率关系:2v(O2)=3v(SO2)
b. 气体密度随着PbS的质量增加而增大
c. 每生成1.5molO2,同时消耗1molSO2
d. 压缩体积到新平衡,浓度增大的倍数:O2>SO2

(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随通入SO2的体积变化如图所示。该微粒X为_________。SO2过量时溶液中仍存在微粒X,解释原因。______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于pH=3的CH3COOH溶液的叙述正确的是
A. 溶液中H2O电离出的c(OH)=1.0×103 mol·L1
B. 加入少量CH3COONa固体后,溶液pH升高
C. 加0.1 mol·L1 CH3COONa溶液使pH>7,则c(CH3COO)=c(Na+)
D. 与等体积pH=11的NaOH溶液混合,所得溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分为CH4,可将CH4设计成燃料电池,来解决能源问题,装置如图所示。在标准状况下,持续通入甲烷,消耗甲烷VL。下列说法错误的是

A. 当0<V≤33.6 L时,负极反应式为CH4+10OH--8e-== CO32-+7H2O
B. 正极反应式为O2 +4H+ +4e-==2H2O
C. 当V=67.2 L时,电池总反应方程式可写为CH4+2O2+NaOH== NaHCO3+2H2O
D. 电解质溶液中的Na+向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com