
【题目】向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl—,降低对电解的影响,反应原理如下:
Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ΔH1=a kJ·mol-1
2Cu+(aq) ΔH1=a kJ·mol-1
Cl—(aq)+Cu+(aq)![]() CuCl(s) ΔH2=b kJ·mol-1
CuCl(s) ΔH2=b kJ·mol-1
实验测得电解液pH对溶液中残留c(Cl—)的影响如图所示。下列说法正确的是

A. 溶液pH越大,Ksp(CuCl)增大
B. 向电解液中加入稀硫酸,有利于Cl-的去除
C. 反应达到平衡增大c(Cu2+),c(Cl—)减小
D. ![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl—(aq)
Cu2+(aq)+Cl—(aq)![]() CuCl(s)的ΔH=(a+2b) kJ·mol-1
CuCl(s)的ΔH=(a+2b) kJ·mol-1
【答案】C
【解析】A. Ksp(CuCl)只与温度有关,与溶液pH无关,故A错误;B. 根据图像,溶液的pH越小,溶液中残留c(Cl—)越大,因此向电解液中加入稀硫酸,不利于Cl-的去除,故B错误;C. 根据Cu(s)+Cu2+(aq)![]() 2Cu+(aq),增大c(Cu2+),平衡正向移动,使得c(Cu+)增大,促进Cl—(aq)+Cu+(aq)
2Cu+(aq),增大c(Cu2+),平衡正向移动,使得c(Cu+)增大,促进Cl—(aq)+Cu+(aq)![]() CuCl(s)右移,c(Cl—)减小,故C正确;D.①Cu(s)+Cu2+(aq)
CuCl(s)右移,c(Cl—)减小,故C正确;D.①Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ΔH1=a kJ·mol-1,②Cl—(aq)+Cu+(aq)
2Cu+(aq) ΔH1=a kJ·mol-1,②Cl—(aq)+Cu+(aq)![]() CuCl(s) ΔH2=b kJ·mol-1,根据盖斯定律,将①×
CuCl(s) ΔH2=b kJ·mol-1,根据盖斯定律,将①×![]() +②得:
+②得: ![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl—(aq)
Cu2+(aq)+Cl—(aq)![]() CuCl(s)的ΔH=(
CuCl(s)的ΔH=(![]() +b) kJ·mol-1,故D错误;故选C。
+b) kJ·mol-1,故D错误;故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列解释实验事实的方程式正确的是
A. Al2(SO4)3溶液滴加氨水产生白色胶状沉淀: Al3++3OH- = Al(OH)3↓
B. 90 ℃时,测得纯水中c(H+)·c(OH-) =3.8×10—13:H2O(l)H+(aq)+OH-(aq)△H<0
C. 除去BaCO3中少量的BaSO4的方法是加入足量饱和的Na2CO3溶液中充分搅拌、过滤、洗涤:BaSO4(s)+CO32-(aq) ![]() BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
D. 碳酸钠溶液滴入酚酞变红:CO32 -+ 2H2O H2CO3+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲是一种利用微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是
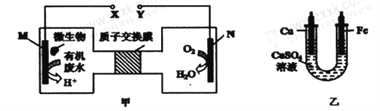
A. 铁电极应与Y相连接
B. H+透过质子交换膜由右向左移动
C. 当N电极消耗0.25mol气体时,则铁电极增重16g
D. M电极反应式:H2NCONH2+H2O-6e-=CO2↑+N2+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 电解熔融NaCl:2Cl-+2H2O ![]() 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B. 用氨水溶解AgCl沉淀:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O
C. Na2CO3溶液吸收溴蒸气:3CO32-+Br2=Br-+BrO3-+3CO2
D. 金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。
(1)己知:N2 (g) +O2 (g) =2NO (g) △H=+180.5kJ·mol-1
C (s) +O2 (g) =CO2 (g) △H=-393.5 kJ·mol-1
2C (s) +O2(g) =2CO (g) △H=-221 kJ·mol-1
若某反应的平衡常数表达式为: 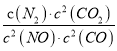 ,请写出此反应的热化学方程式___________________。
,请写出此反应的热化学方程式___________________。
(2)用CH4催化还原NOx可以消除污染,若将反应CH4+2NO2=CO2+2H2O+N2设计为原电池,电池内部是掺杂氧化钇的氧化锆晶体,可以传导O2-,则电池的正极反应式为_______。
(3)利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g) ![]() CH2=CH2(g)+4H2O(g)己知不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是_______(填序号)。
CH2=CH2(g)+4H2O(g)己知不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是_______(填序号)。
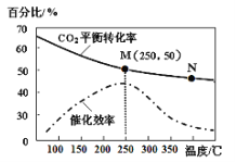
①不同条件下反应,N点的速率最大
②M点时平衡常数比N点时平衡常数大
③温度低于250℃时,随温度升高乙烯的产率增大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(4)在密闭容器中充入5mol CO和4mol NO,发生上述(1)中某反应,如图为平衡时NO的体积分数与温度、压强的关系。
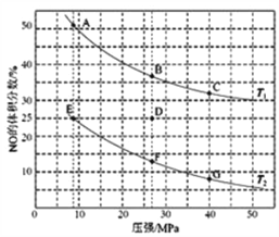
回答下列问题:
①温度:T1______ T2(填“<”或“>”)。
②某温度下,若反应进行到10分钟达到平衡状态D点时,容器的体积为2L,则此时的平衡常数K=______(保留两位有效数字);用CO的浓度变化表示的平均反应速率V(CO)=________。
③若在D点对反应容器升温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中的_______点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是____________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式是_________________________;
负极的电极反应式是_________________________。
(3)右图是一个电解过程示意图。
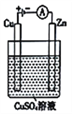
①锌片上发生的电极反应式是______________________。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化为128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com