
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.将1mol氯化铁完全溶于水制成胶体,其中所含胶体粒子数目小于NA
B.标准状况下22.4 L HF中含有的氟原子数目为NA
C.常温下,2.8g C2H4与C3H6的混合物中共价键数为0.6NA
D.1L含NA个Al3+的Al(NO3)3液中,NO3-物质的量浓度大于3 mol/L
【答案】B
【解析】
A. 氢氧化铁胶粒为多个氢氧化铁的聚集体,故1mol氯化铁形成的胶粒的个数小于NA个,故A正确;
B. 标准状况下,HF不是气态,22.4L不是1mol,氟原子数目不是NA,故B不正确;
C.C2H4和C3H6中,每个C原子平均形成了1个碳碳键、每个H原子平均形成了1个碳氢键,2.8g的C2H4和C3H6的混合物中含有2.8![]() 14=0.2molCH2,含0.2mol碳碳键、0.4mol碳氢键,所以共价键数为0.6NA个,故C正确;
14=0.2molCH2,含0.2mol碳碳键、0.4mol碳氢键,所以共价键数为0.6NA个,故C正确;
D.Al3+是弱碱阳离子,在溶液中会水解,故当含NA个Al3+时,溶液NO3-物质的量大于3 mol,其浓度大于3mol/L,故D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】在一定条件下的定容密闭容器中,发生反应2SO2(g)+ O2(g) ![]() 2SO3(g), 下列哪种情况,能表明反应达到平衡状态
2SO3(g), 下列哪种情况,能表明反应达到平衡状态
A. SO3的体积百分含量保持不变
B. SO2速率是O2速率的2倍
C. SO3的浓度是O2浓度的2倍
D. 单位时间内SO2消耗的浓度等于SO3生成的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是

A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03
C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
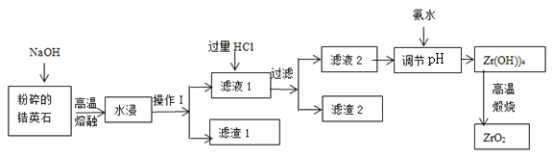
【题目】氧化锆(ZrO2)材料具有高硬度、高熔点、高强度、高韧性、极高的耐磨性及耐化学腐蚀性等优良的物化性能。以锆英石(主要成分为 ZrSiO4,含有少量Al2O3、SiO2、Fe2O3等杂质)为原料通过碱熔法制备氧化锆(ZrO2)的流程如下:
25℃时,有关离子在水溶液中沉淀时的pH数据:
Fe(OH)3 | Zr(OH)4 | Al(OH)3 | |
开始沉淀时pH | 1.9 | 2.2 | 3.4 |
沉淀完全时pH | 3.2 | 3.2 | 4.7 |
请回答下列问题:
(1)流程中旨在提高化学反应速率的措施有________________________________。
(2)操作I的名称是__________________,滤渣1成分为_________,滤渣2的成分为_____________。
(3)锆英石经“高温熔融”转化为Na2ZrO3,写出该反应的化学方程式:____________________。
(4)“调节pH”时,合适的pH范围是__________________。为了得到纯的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是__________________。
(5)写出“高温煅烧”过程的化学方程式________________________________。根据ZrO2的性质,推测其一种用途________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
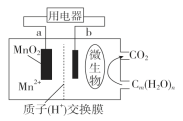
A. 电池工作时,电子由a流向b
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e-===Mn2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子团SCN化合价为-1价,在很多方面跟卤素原子相似,因此称为“拟卤素”。拟卤素离子与卤离子还原性强弱顺序为Cl-<Br-<SCN-<I-,又知氧化性I2>S,下列反应不正确的是( )
A. (SCN)2+2Br-=Br2+2SCN-
B. (SCN)2+H2S=2H++2SCN-+S↓
C. 4H++2SCN-+MnO2![]() Mn2++(SCN)2↑+2H2O
Mn2++(SCN)2↑+2H2O
D. (SCN)2+2I-=2SCN-+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4![]() FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
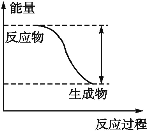
(1)该反应为____________(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是____________(填字母)。
A.改铁片为铁粉B.改稀硫酸为98%的浓硫酸C.升高温度D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____________(填“正”或“负”)极。铜片上产生的现象为____________,该极上发生的电极反应为____________,铁电极的电极反应为____________,外电路中电子由____________(填“正”或“负”,下同)极向____________极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属与硝酸的反应,实验如下。

(1)Ⅰ中的无色气体是_________。
(2)Ⅱ中生成H2的离子方程式是______________________________________。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于NO3-,所以NO3-没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是_______________________________。
②乙同学通过分析,推测出NO3-也能被还原,依据是___________________________,进而他通过实验证实该溶液中含有NH4+,其实验操作是__________________________
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有_________________________试推测还可能有哪些因素影响_________(列举1条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)H2O的相对分子质量是______;1 molH2O质量是______克;1.5 mol H2O的质量为_____;H2O的摩尔质量是_____。
(2)3.01×1022个OH-的物质的量为____mol,质量为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com