
 nY(g) ��H��Q kJ��mol-1����Ӧ�ﵽƽ��ʱ��X�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��
nY(g) ��H��Q kJ��mol-1����Ӧ�ﵽƽ��ʱ��X�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��| �������/L c(X)/mol��L��1 �¶�/�� | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0. 90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g) ��H����Q kJ/mol�����SO2��ת����Ϊ90%�����ڴ������·�Ӧ�ų�������Ϊ
2SO3(g) ��H����Q kJ/mol�����SO2��ת����Ϊ90%�����ڴ������·�Ӧ�ų�������Ϊ| A��2Q kJ | B��Q kJ | C��1.8Q kJ | D��0.9Q kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
| ���� | �� | �� |
| �ݻ���L�� | 0.5 | 0.5 |
| ��Ӧ���ȣ�kJ�� | Q1 | Q2 |
| ��Ӧ����ʼ�� | 1 molA 1 molB | 0.5 molA 0.5 molB |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ��
N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ�� | A��ƽ��������Ӧ�����ƶ� |
| B��ƽ�ⳣ��K���� |
| C��NO2��ת���ʱ�С |
| D��������������ɫ�ȱ�����dz������ԭ����Ҫdz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C��g��+D��g����������ʼŨ�������A��B���ڴﵽƽ��Ĺ����п������������������ͼ��ʾ�������ж�����ȷ����
C��g��+D��g����������ʼŨ�������A��B���ڴﵽƽ��Ĺ����п������������������ͼ��ʾ�������ж�����ȷ����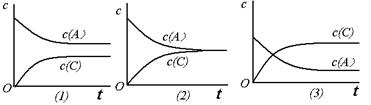
| A����1����K<1 | B����2����K��1 | C����3����K>1 | D���������ֿ���ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Z(g)+W(s) ��H>0������������ȷ����
Z(g)+W(s) ��H>0������������ȷ����| A����������W���淴Ӧ�������� |
| B��������������ѹǿ����ʱ����Ӧ�ﵽƽ�� |
| C�������¶ȣ�ƽ�������ƶ� |
| D��ƽ������X��������Ӧ�Ħ�H���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 qZ(g) ��H��0����һ��������ܱ������дﵽƽ�⣬�����������䣬����������ȷ����
qZ(g) ��H��0����һ��������ܱ������дﵽƽ�⣬�����������䣬����������ȷ����| A���������������Ϊԭ��һ�룬c(Z)Ϊԭ����1.8������m+n��q |
| B���÷�Ӧ�ﵽƽ��ʱ������Y���÷�Ӧ�Ħ�H�ı����� |
| C�������¶ȣ�c(Y)/c(Z)��ֵ��С |
| D��ʹ�ô������Ϳɷ�Ӧ��ȫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ����
2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C��g����һ��ʱ���ﵽƽ�⣬����n mol C������˵����ȷ��
2C��g����һ��ʱ���ﵽƽ�⣬����n mol C������˵����ȷ��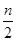 ��
���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com