
【题目】维生素可根据其溶解性的不同分为________性维生素和________性维生素两大类。
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe3O4的混合物中加入100mL1molL﹣1的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现.若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
A.11.2g B.5.6g C.2.8g D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质分子结构的多样性,决定了蛋白质分子具有多种重要功能。如淀粉酶、胃蛋白酶在消化中的________功能,胰岛素可以对糖类物质的代谢具有________功能,免疫球蛋白在人体中的_________功能等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组粒子能在指定溶液中大量共存的是
A. 银氨溶液中:Na+、H+、NO3- B. 碘化钾溶液中:H+、H2O2、SO32-
C. 氢氧化钙溶液中:Na+、ClO-、HCO3- D. 偏铝酸钠溶液中:K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:C(s)+H2O(g)![]() CO(g)+H2 (g) ΔH>0, 某温度下,向5 L密闭容器中加入2 mol C(s)与1 mol H2O(g),t1 s时,CO的物质的量为0.20 mol,到第t2 s时恰好达到平衡,此时CO的物质的量为0.35 mol ,下列说法正确的是( )
CO(g)+H2 (g) ΔH>0, 某温度下,向5 L密闭容器中加入2 mol C(s)与1 mol H2O(g),t1 s时,CO的物质的量为0.20 mol,到第t2 s时恰好达到平衡,此时CO的物质的量为0.35 mol ,下列说法正确的是( )
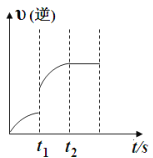
A. t1时改变的条件可能是使用催化剂
B.t1时改变的条件可能是增大 H2O 浓度
C.t1~t2这段时间内的化学反应速率 v(H2O)= 0.15/(t2-t1)
D.t2后继续加入 2 mol C(s)平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将16.1g某元素的含结晶水的硫酸盐晶体,加热后失去全部结晶水变为7.1g,该无水硫酸盐的式量为142,则该晶体(AxH2O)中的x值为( )
A.10 B.9 C.8 D.11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+ 550 kJ/mol,它由两步反应组成:
i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ/molii.SO3(g)分解。
(1)SO3(g)分解的热化学方程式为________________。
(2)工业上常用SO2制备Na2S2O3,向0.1 mol/L的Na2S2O3溶液中滴加稀硫酸的离子方程式为_________。
(3)反应ii的△S_______________0(填 “>”、 “<”、 “=”)。
(4)对反应ii,可用V2O5 作催化剂。已知:SO2+V2O5![]() SO3+V2O4 K1、1/2O2+V2O4
SO3+V2O4 K1、1/2O2+V2O4![]() V2O5 K2, 则在相同温度下,2SO3(g)
V2O5 K2, 则在相同温度下,2SO3(g)![]() 2SO2(g)+O2(g)的平衡常数 K=______________(用K1、K2表示)。
2SO2(g)+O2(g)的平衡常数 K=______________(用K1、K2表示)。
(5) L(L1、L2),X可分别代表压强或温度,右图表示L一定时,反应ii中SO3(g)的平衡转化率随X的变化关系。

①X代表的物理量是_________________;
②比较L1、L2的大小_________________。
(6)维持体系总压p恒定,在T oC时,物质的量为9 mol、体积为2L的SO3(g)发生反应:2SO3(g)![]() 2SO2(g)+O2(g), 已知SO3的平衡转化率25%,则在该温度下反应的平衡常数K=_____________(用最简分数表示)。
2SO2(g)+O2(g), 已知SO3的平衡转化率25%,则在该温度下反应的平衡常数K=_____________(用最简分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的应用正确的是( )
A. 液氨汽化时要吸收大量的热,可用作制冷剂
B. 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
C. 生石灰能与水反应,可用来干燥氯气
D. 氯化铝是一种电解质,可用电解法制铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com