
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各化学式进行解答本题.
解答 解:N2O 中氧为-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得2x-2=0,解得x=+1价;
NaH中钠为+1价,设氢元素的化合价是x,根据在化合物中正负化合价代数和为零,可得,+1+x=0,解得x=-1价;
H2O2中氢为+1价,设氧元素的化合价是x,根据在化合物中正负化合价代数和为零,可得2×1+2x=0,解得x=-1价;
KO2中钾为+1价,设氧元素的化合价是x,根据在化合物中正负化合价代数和为零,可得2x+1=0,解得x=-$\frac{1}{2}$价;
KClO4 钾元素显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零:(+1)+x+(-2)×4=0,解得y=+7;
NaS2O3 钠元素显+1价,氧元素显-2价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零:(+1)+2x+(-2)×3=0,解得x=+$\frac{5}{2}$;
K2MnO4 钾元素显+1价,氧元素显-2价,设锰元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,解得x=+6;
K2Cr2O7钾元素显+1价,氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x+(-2)×7=0,解得x=+6;
Mn2O7氧元素显-2价,设锰元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×7=0,解得x=+2价;
Fe3O4氧元素显-2价,设铁元素化合价为x,根据在化合物中正负化合价代数和为零,可得:3x+(-2)×4=0,解得x=+$\frac{8}{3}$价;
故答案为:+1;-1;-1;+$\frac{1}{2}$;+7;+$\frac{5}{2}$;+6;+7;+$\frac{8}{3}$;
点评 本题考查元素化合价判断,难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.


科目:高中化学 来源: 题型:解答题
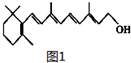
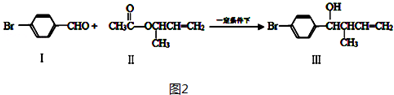

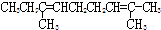 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉可长期放置在烧杯中 | |
| B. | 金属钠燃烧时不能用水灭火,应该用沙子灭火 | |
| C. | 氯水可以用无色透明的试剂瓶装保存 | |
| D. | 实验后剩余的钠不可放回原试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
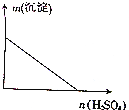 向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )
向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )| A. | 硝酸钙与硫酸钾的混合液 | B. | 氯化钡与碳酸钠的混合液 | ||
| C. | 硫酸镁与氢氧化钾的混合液 | D. | 氯化铝与硝酸钠的混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
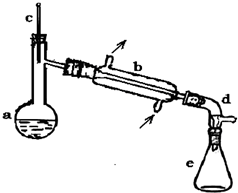 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应 和实验装置如图:
和实验装置如图:| 相对分子质量 | 密度/(g?cm-3 ) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com