
【题目】氯化钙常用于道路融冰剂和干燥剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al2O3、Fe2O3等杂质)制备氯化钙的主要流程如下:
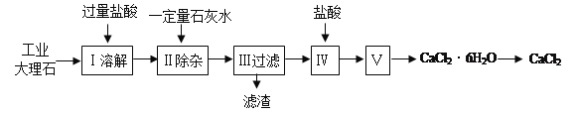 完成下列填空:
完成下列填空:
(1)上述使用的盐酸的物质的量浓度约为6.0mol/L,若用36.5%的盐酸(密度为1.2g/mL)配置6.0mol/L的盐酸100mL,所需的玻璃仪器有玻璃棒、量筒、胶头滴管、 ;需要量取36.5%的盐酸 mL;配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是 。
A.定容摇匀后发现液面低于刻度线 |
B.定容时俯视容量瓶的刻度线 |
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就转入定容操作 |
D.如果加水超过了刻度线,取出少量水使液面恰好到刻度线 |
(2)步骤Ⅰ中有关反应的离子方程式有: 、 、 。
(3)步骤Ⅱ控制石灰水用量的目的是防止(用离子方程式表示): 。
(4)滤渣的主要成分有(写化学式) 。
(5)步骤Ⅴ所含的操作依次是 、 。
(6)制得的氯化钙可以通过如下步骤测定其纯度:
①称取5.5g无水氯化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤;④ 、 ;⑤称量。若得到4.3g碳酸钙,则氯化钙的质量分数为 ;若实验操作规范而测定结果偏低,其原因是 。
【答案】(1)烧杯、100ml容量瓶(各1分,多写1个扣1分,容量瓶没有写规格0分);50(2分);CD(2分、写对一个得1分,写错一个0分)
(2)CaCO3+2H+=Ca2++H2O+CO2↑(2分);Al2O3+6H+=2Al3++3H2O(2分);Fe2O3+6H+=2Fe3++3H2O(2分);
(3)Al(OH)3+OH-=AlO2-+2H2O(2分)
(4)Al(OH)3、Fe(OH)3(2分、写对一个得1分,写错一个0分)
(5)蒸发浓缩,冷却结晶(各1分)
(6)洗涤、干燥(各1分);87%(2分);洗涤时,有少量的碳酸钙溶解(2分)
【解析】试题分析:(1)要配制100ml6mol/L的盐酸,所需的玻璃仪器除了玻璃棒、量筒、胶头滴管外,还需要稀释用到的烧杯,转移时用到的100ml容量瓶。由于在稀释过程中溶质的质量不变,所以还需要量取36.5%的盐酸的体积为![]() =50ml。根据cB=
=50ml。根据cB=![]() 可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大,据此可以判断。A、定容摇匀后发现液面低于刻度线属于正确现象,浓度不变;B、定容时俯视容量瓶的刻度线,则容量瓶中溶液的体积减少,浓度偏高;C、将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就转入定容操作,则溶质的物质的量减少,测定结果偏低;D、如果加水超过了刻度线,取出少量水使液面恰好到刻度线,则导致溶质的物质的量减少,测定结果偏低,因此正确的答案选CD。
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大,据此可以判断。A、定容摇匀后发现液面低于刻度线属于正确现象,浓度不变;B、定容时俯视容量瓶的刻度线,则容量瓶中溶液的体积减少,浓度偏高;C、将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就转入定容操作,则溶质的物质的量减少,测定结果偏低;D、如果加水超过了刻度线,取出少量水使液面恰好到刻度线,则导致溶质的物质的量减少,测定结果偏低,因此正确的答案选CD。
(2)由于碳酸钙、氧化铁、氧化铝均能和盐酸反应,所以步骤Ⅰ中有关反应的离子方程式有CaCO3+2H+=Ca2++H2O+CO2↑、Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O。
(3)由于氢氧化铝是两性氢氧化物,能溶于强碱溶液中。所以步骤Ⅱ控制石灰水用量的目的是防止氢氧化钙过量溶解生成的氢氧化铝,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O。
(4)由于溶液中的Al3+、Fe3+均和氢氧化钙反应生成Al(OH)3、Fe(OH)3沉淀,因此滤渣的主要成分是Al(OH)3、Fe(OH)3。
(5)步骤Ⅴ的主要目的是得到氯化钙晶体,所以所含的操作依次是蒸发浓缩,冷却结晶。
(6)沉淀过滤出来后需要洗涤并干燥。4.3g碳酸钙的物质的量=4.3g÷100g/mol=0.043mol,根据原子守恒可知氯化钙的物质的量也是0.043mol,则氯化钙的质量=0.043mol×111g/mol=4.773g,因此氯化钙的纯度=![]() ×100%=86.78%。碳酸钙不溶于水是相对的,不可能绝对不溶。由于在洗涤时,有少量的碳酸钙溶解,从而导致测定结果偏低。
×100%=86.78%。碳酸钙不溶于水是相对的,不可能绝对不溶。由于在洗涤时,有少量的碳酸钙溶解,从而导致测定结果偏低。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】13C—NMR(核磁共振)可用于含碳化合物的结构分析。下列有关13C的说法不正确的是( )
A. 13C的质量数是13, 核内有6个电子
B. 13C 与12C是两种不同的核素
C. 13C 与12C互为同位素
D. 13C 与12C 的化学性质有很大的差别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. 用灼烧的方法可以区分蚕丝和人造纤维
B. 食用油反复加热会产生稠环芳香烃等有害物质
C. 福尔马林可用来浸制标本,因其可使蛋白质变性
D. 医用消毒酒精中乙醇的浓度为95%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O![]() 6Cu+SO2↑,关于该反应的说法中正确的是
6Cu+SO2↑,关于该反应的说法中正确的是
A. 该反应的氧化剂只有Cu2O
B. Cu2S在反应中既是氧化剂,又是还原剂
C. Cu既是氧化产物又是还原产物
D. 每生成19.2gCu,反应中转移0.6 mole![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. MnO2+4HCl![]() MnCl2 +Cl2↑ + 2H2O中,氧化剂和还原剂物质的量之比为1∶4
MnCl2 +Cl2↑ + 2H2O中,氧化剂和还原剂物质的量之比为1∶4
B. 2H2S+ SO2=3S+2H2O中,氧化产物和还原产物物质的量之比为1∶1
C. 3S+ 6KOH=2K2S+ K2SO3+3H2O中,被氧化和被还原的硫元素物质的量之比为2∶1
D. 5NH4NO3=4N2↑ +2HNO3+9H2O中,反应中发生氧化反应和发生还原反应的氮元素物质的量之比为5∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如下图装置研究电化学原理,下列说法中错误的是( )

A. 若开始时开关K与a连接,其反应与钢铁的吸氧腐蚀类似
B. 若开始时开关K与b连接,则该装置是化学能转变为电能
C. 若开始时开关K与b连接,则标准状况下B极产生2.24 L气体,转移电子0.2 mol
D. 若开始时开关K与b连接,其原理类似于钢铁防护中外加电流的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。
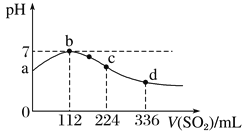
下列分析正确的是
A. 原H2S溶液的物质的量浓度为0.05 mol/L
B. 氢硫酸的酸性比亚硫酸的酸性强
C. b点水的电离程度比c点水的电离程度大
D. a点对应溶液的导电性比d点强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子显电中性的原因是( )
A. 构成原子的各种微粒均不带电
B. 原子核外电子数大于核内质子数
C. 原子核所带电量和核外电子的电量相等,但电性相反
D. 核内质子数等于核电荷数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数98%密度为1.84 g·cm-3浓H2SO4来配制450 mL、0.2 mol·L-1的稀H2SO4.可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有________(填代号)。
(2)经计算,需浓H2SO4的体积为________。现有① 5 mL ②10 mL ③20 mL ④50 mL三种规格量筒,你选用的量筒是_____。
(3)补充整个配制过程的步骤:计算—称量—溶解—_______—______—摇匀。
(4)在配制过程中,其他操作都准确,下列操作中:错误的是_____,能引起浓度偏高的有___(填代号)。
①将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③洗涤溶解用的烧杯与玻璃棒,并将洗涤液转移到容量瓶中
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,俯视标线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com