
 |
��1�� ��98%����������28%��ϡ���ᣬ����IJ�����������Ͳ�⣬���� �� ��
A. ������ B. �ձ� C. ��ƿ D. ����ƿ
��2����ƽ�������ӷ���ʽ��
�� Fe2+ + �� ClO3�D + �� H+ �� �� Fe3+ + �� Cl�D + ��
��3���ۺ���������Һ��SO42�D��Fe3+���ʵ���֮�Ȳ���3��2��Ϊ�˲ⶨ�ۺ���������SO42�D��Fe3+���ʵ���֮�ȣ�Ӧѡ����Լ��� �� ������ţ���
A. NaOH B. FeSO4 C. BaCl2 D. NaClO3
ʵ��ʱ��Ҫ�ⶨ������Fe2O3�� �� ����������д������Ļ�ѧʽ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| m |
| 233 |
| V |
| 200 |
| m |
| 233 |
| V |
| 200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

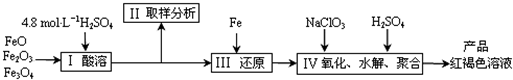
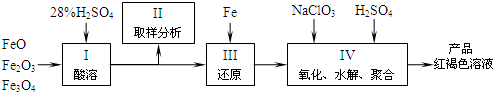
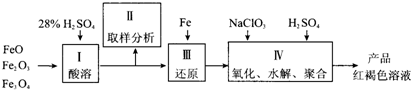
��1����98%����������28%�����ᣬ����IJ�����������Ͳ�⣬���� ��
(a) ����ƿ (b) �ձ� (c) ��ƿ
��2������IIȡ��������Һ�е�Fe2+��Fe3+�ĺ�����Ŀ���� ��
(a) ������Һ��Fe2+��Fe3+������
(b) ȷ����һ����ԭ����������
(c) ȷ������Fe2+����NaClO3����
(d) ȷ������������������ȫ
��3����NaClO3����ʱ��Ӧ����ʽ���£�
6FeSO4 + NaClO3 + 3H2SO4 �� 3Fe2(SO4)3 + NaCl + 3H2O
������HNO3��������Ӧ����ʽ����
6FeSO4 + 2HNO3 + 3H2SO4 �� 3Fe2(SO4)3 + 2NO�� + 4H2O
��֪1mol HNO3�۸�0.16Ԫ��1mol NaClO3�۸�0.45Ԫ��������HNO3����NaClO3���������ĵñף����� ������ ��
�ۺ���������Һ��SO42����Fe3+���ʵ���֮�Ȳ���3:2���������й�ѡ����Լ��ͻ����������ⶨ�ۺ���������Ʒ��Һ��SO42����Fe3+���ʵ���֮�ȡ�
��4���ⶨʱ������Լ� ��
(a) NaOH (b) FeSO4 (c) BaCl2 (d) NaClO3
��5����Ҫ�ⶨ �� ����������д������Ļ�ѧʽ����
��6��ѡ���ⶨ����������Ļ������� ���������Ⱥ�˳���г�����
(a) ��ȡ����Һ (b) ���ˡ�ϴ�� (c) �������ᾧ
(d) ��ȴ������ (e)��ɻ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com