
【题目】①![]() 和
和![]() ②红磷和白磷 ③
②红磷和白磷 ③![]() 和
和![]() ④
④![]() 和
和![]() ⑤
⑤![]() 和
和![]() ⑥
⑥ 和
和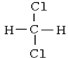
(1)属于同素异形体的是________(2)互为同位素的是________
(3)互为同分异构体的是________(4)属于同系物的是________
(5)属于同种物质的是________
【答案】②⑤ ① ④ ③ ⑥
【解析】
同位素是指质子数相同、中子数不同的同一种元素的不同核素互称为同位素;分子式相同结构不同的化合物互为同分异构体;性质和结构都完全相同的是同一种物质;由同一种元素形成的不同单质互为同素异形体;结构相似、分子组成相差若干个CH2原子团的同一类有机物互称为同系物。据此解答。
(1)红磷和白磷是磷元素形成的不同单质,互为同素异形体。氧气和臭氧是氧元素形成的不同单质,互为同素异形体;
(2)16O和18O的质子数相同中子数不同,互为同位素;
(3)CH3CH2CH2CH3和CH3CH(CH3)CH3的分子式相同,结构不同,互为同分异构体;
(4)![]() 和CH3CH2CH2CH3均是烷烃,结构相似,分子组成上相差2个CH2,二者互为同系物;
和CH3CH2CH2CH3均是烷烃,结构相似,分子组成上相差2个CH2,二者互为同系物;
(5) 和
和 的结构和性质完全相同,属于同种物质。
的结构和性质完全相同,属于同种物质。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去)。

I.若A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种常见无色无味的有毒气体,B、E均为汽车尾气成分。
(1)写出反应①的化学方程式____________。
(2)写出B和E在催化剂条件下生成C的化学方程式______________。
II.若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10电子粒子;E为澄清石灰水。
(1)写出反应②的化学方程式_____________。
(2)将一定量的气体D通入2L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。

①O点溶液中所含溶质的化学式为_______,横坐标3-5段发生的离子方程式为_____。
②标况下,通入气体D的体积为______L,C溶液的物质的量浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)![]() N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.

(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4) |
B.容器内压强不再发生变化 |
C.X的体积分数不再发生变化 |
D.容器内气体原子总数不再发生变化 |
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A. υ(C)=4 mol·(L·s)-1B. υ(B)=6 mol·(L·s)-1
C. υ(A)=3 mol·(L·s)-1D. υ(D)=2mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
I.某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、 Fe3+、 Al3+、 Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:

注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________(填序号);已知钠离子交换树脂的原理:Mn++nNaR→MRn+nNa+,此步操作被交换除去的杂质离子是____(填序号)。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程中,每消耗172.8gCr2O72-转移4.8 mol e-,该反应离子方程式为________。
Ⅱ.酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处 理含Cr2O72-的废水。
实验室用如图装置模拟处理含Cr2O72-废水,阳极反应是Fe-2e-=Fe2+,阴极反应式2H++2e-=H2↑随着电解进行,阴极附近pH升高。

(1)电解时能否用Cu电极来代替Fe电极?____(填“能”或“不能”), 理由是______________。
(2)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为________________。
(3)上述反应得到的金属阳离子在阴极区可沉淀完全,从其对水的电离平衡影响角度解释其原因__________。
(4)若溶液中初始含有0.lmol Cr2O72-,则生成的阳离子全部转化成沉淀的质量是_____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式为: ,则用Na、NaOH、NaHCO3与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为 ( )
,则用Na、NaOH、NaHCO3与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为 ( )
A. 3∶3∶2 B. 3∶2∶1 C. 1∶1∶1 D. 3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式不正确的是
A. 钠与水反应:2Na+2H2O![]() 2Na++2OH–+H2↑
2Na++2OH–+H2↑
B. 向碳酸氢铵溶液中加入足量石灰水: Ca2++HCO3+OH–![]() CaCO3↓+H2O
CaCO3↓+H2O
C. 向氢氧化钡溶液中加入稀硫酸: Ba2++2OH +2H++SO42![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 泡沫灭火器反应原理:3HCO3+Al3+![]() 3CO2↑+Al(OH)3↓
3CO2↑+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中既能跟稀盐酸反应,又能跟氢氧化钠溶液反应的是
①NaHCO3 ②Al ③Al(OH)3 ④MgO
A.②③B.①②③C.②③④D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式___________________________________,写出基态24Cr原子的价电子排布式________________________;
(2)写出基态N的原子核外电子排布图:__________________;
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了_______________________;
(4)Fe3+比Fe2+的稳定性更________(填“强”或“弱”),从结构上分析原因是____________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com