
����Ŀ��������G��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ������ͨ����ͼ��ʾ��·�ߺϳ�

��֪��RCOOH ![]() RCOCl��D��FeCl3��Һ�ܷ�����ɫ��
RCOCl��D��FeCl3��Һ�ܷ�����ɫ��
(1)A��B�ķ�Ӧ������___________��B��C��ת�����ӵ��Լ��ٿ�����______��
(2)E�Ľṹ��ʽΪ_________��
(3)F������NaOH��Һ��ַ�Ӧ�Ļ�ѧ����ʽΪ_________________��
(4)д��ͬʱ������������������E��ͬ���칹��Ľṹ��ʽ____________��
���ܷ���ˮ�ⷴӦ����FeCl3��Һ�ܷ�����ɫ��Ӧ�۱����������ֲ�ͬ��ѧ��������ԭ��
(5)��֪�����ǻ�һ�㲻��ֱ���������������������ᱽ������![]() ����һ����Ҫ���л��ϳ��м��塣��д���Ա��ӡ��ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ(��ԭ������)��
����һ����Ҫ���л��ϳ��м��塣��д���Ա��ӡ��ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ(��ԭ������)��
ע���ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��________________________________

���𰸡� ������Ӧ ���Ƶ�������Һ�����Ƶ�������ͭ����Һ ![]()
![]() +3NaOH
+3NaOH![]()
![]() +CH3COONa+H2O+CH3OH
+CH3COONa+H2O+CH3OH 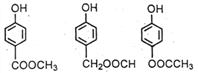
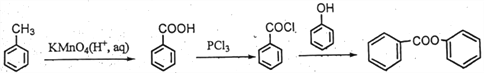
����������F��֪EΪ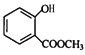 ������D�ķ���ʽ��֪DΪ
������D�ķ���ʽ��֪DΪ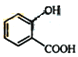 ���ɿ�֪CΪCH3COOH��BΪCH3CHO��AΪCH3CH2OH��(1) A��B��CH3CH2OH������Ӧ����CH3CHO����Ӧ������������Ӧ��B��C��ת������ȩ�������ữת��Ϊ���ᣬ���ӵ��Լ��ٿ��������Ƶ�������Һ�����Ƶ�������ͭ����Һ��(2)E�Ľṹ��ʽΪ
���ɿ�֪CΪCH3COOH��BΪCH3CHO��AΪCH3CH2OH��(1) A��B��CH3CH2OH������Ӧ����CH3CHO����Ӧ������������Ӧ��B��C��ת������ȩ�������ữת��Ϊ���ᣬ���ӵ��Լ��ٿ��������Ƶ�������Һ�����Ƶ�������ͭ����Һ��(2)E�Ľṹ��ʽΪ ��(3) F��
��(3) F��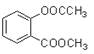 ��������NaOH��Һ��ַ�Ӧ�Ļ�ѧ����ʽΪ
��������NaOH��Һ��ַ�Ӧ�Ļ�ѧ����ʽΪ![]() +3NaOH
+3NaOH![]()
![]() +CH3COONa+H2O+CH3OH��(4) ����E��
+CH3COONa+H2O+CH3OH��(4) ����E�� ����ͬ���칹���ܷ���ˮ�ⷴӦ��˵������������FeCl3��Һ�ܷ�����ɫ��Ӧ��˵���з��ǻ��������������ֲ�ͬ��ѧ��������ԭ�ӣ�˵���Ƕ�λ�ṹ�����Եõ�
����ͬ���칹���ܷ���ˮ�ⷴӦ��˵������������FeCl3��Һ�ܷ�����ɫ��Ӧ��˵���з��ǻ��������������ֲ�ͬ��ѧ��������ԭ�ӣ�˵���Ƕ�λ�ṹ�����Եõ�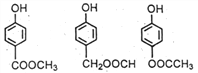 ��(5) �ױ��������ɱ����ᣬ��ȡ�������ȱ���ˮ�����ɱ��ӣ��Դ˺ϳɸ��л���ϳ�����ͼΪ��
��(5) �ױ��������ɱ����ᣬ��ȡ�������ȱ���ˮ�����ɱ��ӣ��Դ˺ϳɸ��л���ϳ�����ͼΪ��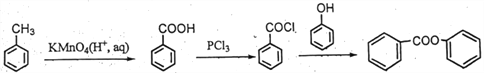 ��
��


 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к�������(C3H6O3)��2 mol��������к���(����)
A. 3 mol��ԭ��
B. 12 mol��ԭ��
C. 6.02��1023��O3����
D. 6.02��1023���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƿ���CO2���ã���0.2molNa218O2��ȫ���ú����ɵ�Na2CO3������Ϊ
A. 21.2g B. 2l.6g C. 22.0g D. 22.4g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ����Ƶ������У�˵����ȷ���ǣ� ��
A. Na��ˮ��Ӧ��Na��Խ������Խ���� B. ��ʵ�������Ʊ�����ʯ���ͻ�ú����
C. Na�ڿ�����ȼ�գ�������Na2O D. Na������ɫ������Ӳ�ȴ��۵��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ�� (����)��
A.1s22s12p1��ʾ���Ǽ���̬ԭ�ӵĵ����Ų�
B.3p2��ʾ3p�ܼ����������
C.ͬһԭ���У�3d���������С��4s���������
D.ͬһԭ���У�2p��3p��4p���ӵ�������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�����La2(CO3)3�ݿ�����������ĩ���������ߵĸ�������Ѫ֢���Ʊ���Ӧԭ��Ϊ��LaC13+6NH4HCO3= La2(CO3)3����6NH4Cl+ 3CO2��+3H2O��ij��ѧ��ȤС����������װ��ʵ������ģ���Ʊ�̼���硣

��l��ʢ��ϡ���������Ϊ____________��
��2���Ʊ�̼����ʵ�������е��ܴ������ҵ�����˳��Ϊ��F��___��___ ��___ ��___ ��___ ��
��3��Y�з�����Ӧ�Ļ�ѧ��ӦʽΪ________________��
��4��X��ʢ�ŵ��Լ���_____��������Ϊ________________��
��5��Z��Ӧ��ͨ��NH3����ͨ�������CO2��ԭ��Ϊ_________��
��6��La2(CO3)3���������IJⶨ��ȷ��ȡ10.0g��Ʒ����������10.0mLϡ�����У�����10 mLNH3 ��NH4Cl������Һ������0.2g������炙��ָʾ������0.5mol/LEDTA��Na2H2Y������Һ�ζ���������ɫ��La3��+H2Y-=LaY-+2H+��������EDTA ��Һ44.0 mL�����Ʒ��La2(CO3)3������������[La2(CO3)3]=_________��
��7���û�ѧ��ȤС��Ϊ̽��La2(CO3)3��La(HCO3)3���ȶ���ǿ������������µ�ʵ��װ�ã�����Թ���ʢ�ŵ�����Ϊ_______��ʵ������У��������Թ��й�������������ʱ��Ĺ�ϵ������ͼ��ʾ��������ʵ������й۲쵽������Ϊ______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������3.01��1023��H��H2O����H2O���ʵ�����________����H2O�к��е��ӵĸ���Ϊ______________��
��2��______mol H2O�к��е���ԭ������1.5 mol CO2�к��е���ԭ������ȡ�
��3���������ʵ�����NH3��CH4��ϣ����������NH3��CH4��������Ϊ________��
��4��ҪʹNH3��CH4����ͬ��Ŀ��Hԭ�ӣ���NH3��CH4�����ʵ���֮��Ϊ__________��
��5����״���£��ܶ�Ϊ0.75 g��L��1��NH3��CH4��ɵĻ�������У�NH3���������Ϊ__________��(ע:���������Ϊ���ʵ���������
��6����֪a g A��b g Bǡ����ȫ��Ӧ����0.4mol C��d g D����C��Ħ������Ϊ________
��7��ͬ�¡�ͬѹ�µ�������SO2�����CO2���壬���֮��___________��ԭ����Ŀ֮��Ϊ___________���ܶȱ�Ϊ___________����Ԫ�ص�������Ϊ__________��
��8��ij��̬�����ﻯѧʽΪRO2���ڱ�״���£�1.28g������������Ϊ448mL������������Ħ������Ϊ____________��R�����ԭ������Ϊ_____________��
��9��200mL��2.0mol/L��Al2��SO4��3��Һ�к�Al3+�����ʵ���Ϊ___________������ȡ��10mL������10mL��Һ��ˮϡ�͵�50mL��������Һ�����������ʵ���Ũ��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������;��˵����,��������� ��
A. SiO2�����õİ뵼����� B. SO2������Ư��ֽ��
C. Na2O2������DZˮͧO2��Դ D. Cl2����������������Ư��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4���ǻ��㶹�أ��Ǻϳ�ҩ�����Ҫ�м��壬�������ϳ�;�����£�

��֪����F�Ľṹ��ʽΪ ��
��
�� ( X=O��N��S��R����)��
( X=O��N��S��R����)��
��RCOOR+2R��OH��R��COOR��+2ROH
�ص��������⣺
(1)����4���ǻ��㶹�ص�˵����ȷ����____________��(����ĸ)
a.��ʹ��ˮ��ɫ b.1mol �������������4mol NaOH��Ӧ
c.�����������9��̼ԭ�ӹ�ƽ�� d.���ڱ���ͬϵ��
(2)A����B�ķ�Ӧ����Ϊ__________��D�Ľṹ��ʽΪ__________��
(3)I������Ϊ_______________��
(4)д��G����H�Ļ�ѧ����ʽ________________________��
(5)������������������F���ṹ��ʽ����֪����ͬ���칹�����Ŀ��__________�֣�
a.�ܷ���������Ӧ b.���ڱ��Ķ�ȡ���� c.ֻ����һ����
д������ͬ���칹������ʹFeCl3��Һ����ɫ���˴Ź���������������������Ϊ1:2:2:2:1�Ľṹ��ʽ______________��
(6)�������֪ʶ����Ϣ�����������ϳ�·�ߣ��Ա���Ϊ��ʼԭ��(���Լ���ѡ)����Ʊ� �ĺϳ�·��______________��
�ĺϳ�·��______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com