
【题目】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:
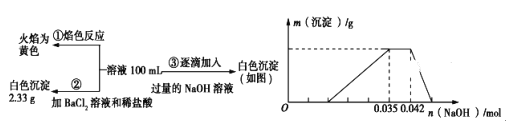
请回答下列问题:
(1)焰色反应是_________ (填“物理”或“化学”)变化;实验②中产白色沉淀是_________ (填化学式)。
(2)原溶液中一定存在的离子有________________,可能存在的离子有________________,一定不存在的离子有________________ (写化学式)。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为________________
(4)若通过实验确定原废水中c(Na+)=0.14 mol·L1,试判断原废水中NO3是否存在?________________(填“存在”“不存在”或“不确定”)。 若存在,c(NO3)=___________mol·L1。(若不存在或不确定则此空不填)
【答案】物理 BaSO4 Na+、SO42-、H+、Al3+、NH4+ NO3- Fe3+、Mg2+、CO32- 1:1 存在 0.36
【解析】
根据溶液颜色及焰色反应等实验现象分析溶液中离子存在情况;根据图像中沉淀的变化及消耗的氢氧化钠的物质的量分析计算溶液中存在的离子及其物质的量;根据溶液的电中性分析判断溶液中可能存在的离子,并计算其物质的量。
(1)焰色反应是物理变化;实验②中加入BaCl2和盐酸,产白色沉淀是不溶液盐酸的BaSO4,故答案为:物理;BaSO4;
(2)Fe3+呈黄色,则肯定不存在,实验①中焰色反应为黄色,则确定存在Na+;实验②中加入BaCl2和盐酸,产白色沉淀是不溶液盐酸的BaSO4,确定存在SO42-,根据实验③中沉淀的变化,可以分析知发生的反应依次为:H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH4H2O、Al(OH)3+OH-=AlO2-+2H2O则确定有H+、Al3+、NH4+,沉淀完全溶解,则没有Mg2+,因为CO32-与Al3+不能共存,所以无CO32-;所以原溶液中一定存在的离子有Na+、SO42-、H+、Al3+、NH4+;一定不存在的离子有Fe3+、Mg2+、CO32-;可能存在的离子是NO3-,故答案为:Na+、SO42-、H+、Al3+、NH4+;NO3-;Fe3+、Mg2+、CO32-;
(3)根据图像中沉淀不变的部分及NH4++OH-=NH4H2O分析知:n(NH4+)=n(OH-)=0.042mol-0.035mol=0.007mol;根据图像中生成沉淀部分及Al3++3OH-=Al(OH)3↓分析知:c(Al3+)=1/3n(OH-)=1/3×(0.042mol-0.035mol)×3=0.007mol,则原溶液中c(NH4+)与c(Al3+)的比值等于物质的量之比:0.007mol:0.007mol=1:1,故答案为:1:1;
(4)根据硫酸钡沉淀2.33g,n(SO42-)=![]() ,根据电荷守恒,阴离子电荷总物质的量为0.01mol×2=0.02mol,阳离子电荷总物质的量为n(H+)+n(Al3+)+n(NH4+)+n(Na+)=0.014mol+0.007×3mol+0.007mol+0.14mol/L×0.1L=0.056mol,则原废水中存在NO3-,c(NO3-)=
,根据电荷守恒,阴离子电荷总物质的量为0.01mol×2=0.02mol,阳离子电荷总物质的量为n(H+)+n(Al3+)+n(NH4+)+n(Na+)=0.014mol+0.007×3mol+0.007mol+0.14mol/L×0.1L=0.056mol,则原废水中存在NO3-,c(NO3-)=![]() =0.36mol/L;故答案为:存在;0.36。
=0.36mol/L;故答案为:存在;0.36。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1 m3(标准状况)CH4按上式完全反应,产生H2_________mol。(精确到0.1)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V m3(标准状况)的取值范围为________。
(3)CH4和H2O(g)及富氧空气(O2含量较高的空气)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比,V(O2):V(N2)=________。
(4)若CH4和H2O(g)及(3)题中的富氧空气混合反应,产物气体中V(H2):V(N2)=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见物质 A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。 下列推断不正确的是 ( )

A. 若D为NaCl,且A可与C反应生成B,则 E 可能是 CO2
B. 若D是一种强碱, 则A、B、C 均可与 X 反应生成 D
C. 若D是一种白色沉淀, 在空气中最终变为红褐色,则 A可能是铁
D. 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。请回答下列问题:
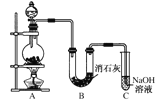
(1)A为实验室制氯气的发生装置,反应化学方程式为_________________________;某学生用12 mol·L-1的浓盐酸100 mL和足量的MnO2反应制Cl2,实际得到的Cl2________6.72 L(填“<”、“>”或“=”)。
(2)漂白粉将在U形管中产生,其化学方程式是_________________________________。
(3)此实验所得漂白粉的有效成分偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是________________。
②Cl2中含HCl,会发生反应2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,可将装置作何改进______________________________。
(4) C装置的作用是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铁溶液可腐蚀印刷电路板.上的铜膜,某教师为了从腐蚀废液(含有大量FeCl3、FeCl2、CuCl2)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用。准备采用下列步骤:
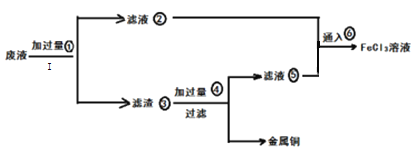
(1)步骤I的操作名称:_________________ :所需玻璃仪器:_______________________
(2)写出FeCl3溶液与铜箔发生反应的离子方程式:__________________________________
(3)检验废腐蚀液中是否含有Fe3+所需试剂:______________________(填名称)
(4)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:_______________________此转化的化学方程式为:___________________________________________________________
(5)写出③中所含物质:__________________(填化学式)⑥发生反应的离子方程式:________
(6)若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是_____(填写编号)
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为探究AgNO3溶液和不同类型盐溶液反应的多样性,设计如图实验:已知:AgSCN为白色难溶物。下列说法不正确的是( )

A.①中的白色沉淀是![]()
B.向①的试管中滴加![]() KI溶液,有黄色沉淀生成证明存在
KI溶液,有黄色沉淀生成证明存在![]()
![]()
![]()
C.②中发生了氧化还原反应
D.对于②中红色褪去的原因可能与平衡移动原理有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基本知识填空
(1)在一定条件下,当一个可逆反应的_____与____相等时,反应物的浓度与生成物的浓度不再改变,即达到化学平衡状态。
(2)化学平衡状态的特征:_____、____、_____、_____、_____。
(3)对于可逆化学反应mA+nBpC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:______。
(4)强电解质包括的范围:____、____、____。弱电解质包括的范围:____、_____、____、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种可充电锂-空气电池如图所示,当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
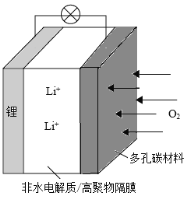
A.充电时,电解质溶液中Li+向多孔碳材料区迁移
B.充电时,电池总反应为Li2O2-x==2Li+(1-![]() )O2
)O2
C.放电时,多孔碳材料电极为负极
D.放电时,外电路电子由多孔碳材料电极流向锂电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com