
【题目】已知X是一种晶体,在一定条件下可发生如图所示的变化。下列叙述正确的是

①X可能是铝或硅 ②X可能是原子晶体或金属晶体
③W一定是两性物质 ④W晶体的熔点很高
A. ①②③ B. ①②④ C. 只有③ D. ③④
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:

下列说法正确的是
A. 分离器中的物质分离操作为过滤
B. 膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率
C. 该工艺中I2和HI的相互转化体现了“碘循环”
D. 碘循环工艺的总反应为2SO2+4H2O+I2 == H2+2H2SO4+ 2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大.A、D同主族,可形成离子化合物X;B的氢化物与F的氢化物可反应生成离子化合物Y,且B的单质是空气中含量最高的物质;C原子的最外层电子是次外层电子数的3倍;D、E、F 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水.
(1)B元素的名称是 , B单质的结构式为 .
(2)用电子式表示化合物X的形成过程 .
(3)化合物Y的电子式为 , A2C2的电子式为 .
(4)D、F最高价氧化物的水化物之间反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在两升密闭容器中进行1分钟后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是( )
A.NO 0.001 molL﹣1
B.H2O 0.002 molL﹣1
C.NH3 0.002 molL﹣1
D.O2 0.0025 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是
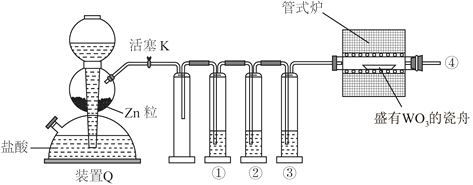
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列说法正确的是( ) 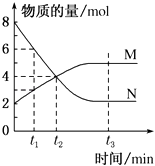
A.反应开始到t2时,反应达到平衡状态
B.反应开始到t1(t1=1s),N的物质的量浓度变化了2mol/L
C.反应开始到t2(t2=2s),用M表示反应速率为0.5mol/(L.s)
D.反应的化学方程式为:N(g)2M(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10﹣10m) | 0.74 | 1.60 | 0.89 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +2 | +5 | +7 | +1 | +5 | +3 | |
﹣2 | ﹣3 | ﹣1 | ﹣3 |
回答下列问题:
(1)③的元素符号是 , ①的元素名称是 .
(2)在这8种元素的最高价氧化物的水化物中,酸性最强的化合物的名称是 . ②与⑤形成的化合物的电子式是: , 属化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用分子式表示) .
(4)写出⑥最高价氧化物对应水化物跟⑧的最高价氧化物反应的离子方程式: .
(5)请设计实验比较单质②⑧的金属性,写出简单的实验步骤和现象: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一体积为2L的恒温恒容密闭容器中充入一定量的H2和N2,发生反应:N2(g)+ 3H2(g) ![]() 2NH3(g) △H=a kJmol-1。体系中气体的物质的量随时间的变化如图所示。
2NH3(g) △H=a kJmol-1。体系中气体的物质的量随时间的变化如图所示。
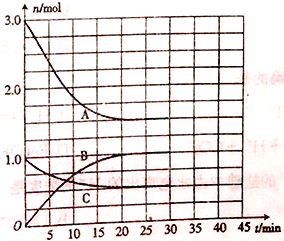
(1)表示N2浓度变化的曲线是________(填“A”“ B”或“C”),25min时,c(NH3)= ______。
(2)0~20min内,v(H2)= ______。若该过程中反应放出的热量为47.2kJ,则a=______。
(3)30min时,向容器中再充入一定量的NH3,一段时间后,与原化学平衡状态时的反应速率相比,正反应速率______(填“增大”“ 减小”或“不变”,下同),逆反应速率_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com