
【题目】已知某微粒的结构示意图为: (y ≠ 0 )。请回答:
(y ≠ 0 )。请回答:
(1)当x-y=10时,该微粒为________(填“原子”、“阳离子”或“阴离子”)。
(2)当y=8时,微粒可能为(不少于5种)___________________。
(3)写出x+y=12与x+y=16的元素最高价氧化物对应水化物相互反应的离子方程式 _。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳、氢元素可形成种类繁多的烃类物质,根据烃类物质的结构与性质,回答下列问题:
Ⅰ.某烯烃的结构简式如下所示,回答下列问题:

(1)用系统命名法对该烃与H2的加成产物命名:__________________,该加成产物的一氯取代物有____种,该加成产物的同分异构体中沸点最低的是_____(写结构简式)。
(2)写出该烯烃与溴的四氯化碳溶液反应的化学方程式__________________。
(3)该烯烃可以加聚生成高分子,写出该高聚物的结构简式________。
Ⅱ.(1)某芳香烃的相对分子质量为 92,该烃的分子式为_______,其结构简式为_____;请写出该烃最简单的同系物与浓硝酸反应的化学方程式:____,反应类型为____。
(2)标准状况下,某气态烷烃和烯烃(含一个双键)的混合气体4.48L完全燃烧后,将产生的气体缓慢通过浓硫酸,浓硫酸增重8.10g,剩余气体通过碱石灰,碱石灰增重13.20g。另再取4.48L标准状况下的该混合气体,将它通入过量的溴水中,溴水增重2.10g。组成混合气体的两种烃及体积分数为____和____(烃写分子式,回答体积分数时指明对应的烃)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有Cl-、Br-和CrO![]() ,浓度均为0.010 mol/L,向该溶液中逐滴加入0.010 mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 ( )
,浓度均为0.010 mol/L,向该溶液中逐滴加入0.010 mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 ( )
A.Cl-、Br-、CrO![]() B.CrO
B.CrO![]() 、Br、Cl-
、Br、Cl-
C.Br-、Cl-、CrO![]() D.Br、CrO
D.Br、CrO![]() 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解质溶液的正确判断是
A.在pH=12的溶液中,K+、Cl-、HCO![]() 、Na+可以共存
、Na+可以共存
B.水电离的c(H+)=1×10-3mol/L的溶液中:Na+、Fe3+、SO42-、Cl-可以共存
C.由0.l moI/L BOH溶液的pH=10,可推知BOH溶液存在BOH = B++OH-
D.![]() =1×10-13mol/L的溶液中:Ba2+、ClO-、Cl-、NO3-可以共存
=1×10-13mol/L的溶液中:Ba2+、ClO-、Cl-、NO3-可以共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌化妆品的主要成分Z具有美白功效,原从杨树中提取,现可用如下图所示反应合成。下列对X、Y、Z的叙述,正确的是

A. X、Y和Z均能和NaOH溶液反应
B. X和Z均能和Na2CO3溶液反应,但不能和NaHCO3溶液反应
C. Y既能发生加聚反应,也能发生缩聚反应
D. Y分子中所有原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依照阿伏加德罗定律,下列叙述正确的是
A. 同温同压下两种气体的体积之比等于摩尔质量之比
B. 同温同压下两种气体的物质的量之比等于密度反比
C. 同温同压下两种气体的摩尔质量之比等于密度反比
D. 同温同体积下两种气体的物质的量之比等于压强之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做同周期元素性质递交规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
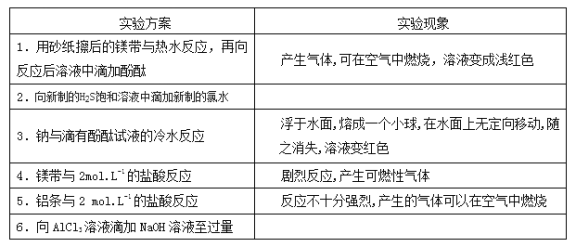
请你帮助该同学整理并完成实验报告
(1)实验目的:验证同周期元素金属性、非金属性的变化规律。
(2)实验用品:略。
(3)实验内容:(填写题给信息表中相应的实验现象,并在有空格处写出相对应的离子方程式)
实验方案 | 实验现象 | 有关离子方程式 |
不填 | 不填 | |
② | ______________ | ______________ |
不填 | ______________ | |
④ | 不填 | 不填 |
⑤ | 不填 | ______________ |
⑥ | ______________ | ______________ |
(4)实验结论:______________。
(5)问题与讨论:
请从原子结构理论上简单说明具有上述结论的原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
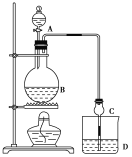
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用是________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:__________。
(2)球形干燥管C的作用是_______________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)________________;反应结束后D中的现象是____________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键
B. 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA
C. lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上
D. 80℃ 时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com