
【题目】如图为某市所售盐酸试剂瓶标签上的部分数据.通过计算回答. 
(1)该盐酸中HCl的物质的量浓度.
(2)将6.50g锌投入足量的该盐酸中,充分反应后生成的H2在标准状况下的体积.
【答案】
(1)解:依据图中所售盐酸试剂瓶标签上数据可知:氯化氢的摩尔质量为:36.5g/mol,密度为1.18g/ml,氯化氢的质量分数为36.5%,则氯化氢的物质的量浓度C= ![]() =
= ![]() =11.8mol/L;
=11.8mol/L;
答:该盐酸中HCl的物质的量浓度11.8mol/L
(2)解:6.50g锌物质的量n= ![]() =0.1mol,盐酸足量,应依据锌的量计算氢气的物质的量,设生成标况下氢气体积为V,则:
=0.1mol,盐酸足量,应依据锌的量计算氢气的物质的量,设生成标况下氢气体积为V,则:
Zn | + | 2HCl | = | ZnCl2 | + | H2↑ |
1 | 22.4L | |||||
0.1mol | V |
解得V=2.24L;
答:将6.50g锌投入足量的该盐酸中,充分反应后生成的H2在标准状况下的体积2.24L
【解析】(1)依据C= ![]() 计算氯化氢的物质的量浓度;(2)依据n=
计算氯化氢的物质的量浓度;(2)依据n= ![]() 金属锌的质量,依据Zn+2HCl=ZnCl2+H2↑计算产生氢气的体积.
金属锌的质量,依据Zn+2HCl=ZnCl2+H2↑计算产生氢气的体积.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种.为检验其中含有的离子,进行如下实验: ①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.
下列关于原溶液的说法正确的是( )
A.肯定存在NH4+、Cl﹣、Br﹣
B.是否存在Na+需要通过焰色反应来确定
C.SO42﹣、SO32﹣至少含有一种
D.肯定不存在Ba2+、Cu2+、SO32﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量为W1g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L.向溶液中逐滴加入浓度为amolL﹣1的HCl溶液,过程中有白色沉淀产生后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2L.将溶液蒸干并充分灼烧得到固体W2g.下列关系式中错误的是( )
A.24n(Al)+35.5n(Na)=W2﹣W1
B.n(Na)+3n(Al)=aV2
C.n(Na)+3n(Al)= ![]()
D.aV2= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰③加盐酸 ④过滤 ⑤熔融电解,正确的生产顺序是( )
A.①②③④⑤
B.⑤④③①②
C.②④③①⑤
D.③④②①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上的海水资源开发利用的部分工艺流程如下图所示:
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜共同允许通过的分子或离子是 , 电解槽中的阳极材料为。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2 , 能否按Br2、Mg(OH)2、CaSO4顺序制备? , 原因是。
(3)溴在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,但在上述工艺中却不用四氯化碳,原因是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理生活污水中的NH4+ , 过程如下: 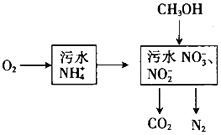
(1)空气将NH4+转变为NO3﹣或NO2﹣ , 溶液pH(填“增大”、“减小”或“不变”).
(2)根据较新的研究表明,将只含NO2﹣的污水与含NH4+的污水按比例混合,直接转化为无毒气体,该气体为 . 此方法的优点是
(3)完全处理含1mol NH4+污水,则n(O2)与n(CH3OH)关系式为[以n(O2)与n(CH3OH)表示].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,w g某物质在足量氧气中充分燃烧,其燃烧产物立即与过量的Na2O2反应,固体质量增加w g.在①H2②CO ③CO和H2的混合气 ④C6H12O6( )
A.均不符合
B.只有①②
C.只有①②③
D.全部符合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置可应用于实验室制氯气并回收二氯化锰的实验,能达到实验目的是( ) 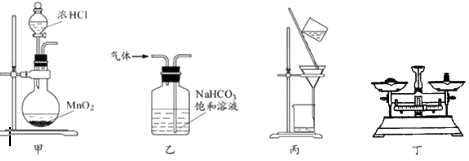
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离出MnCl2溶液中的固体MnO2
D.用装置丁称得回收的二氯化锰质量为5.36g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com