
【题目】下列实验中,能达到相应实验目的的是
|
|
|
|
A.制备并收集乙酸乙酯 | B.证明氯化银溶解度大于硫化银 | C.验证溴乙烷的消去产物是乙烯 | D.推断S、C、Si的非金属性强弱 |
A.AB.BC.CD.D
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】已知某物质X能发生如下转化:
![]()
下列有关上述转化关系中物质及其反应的叙述错误的是( )
A.若X为![]() 或
或![]() ,则A为硝酸
,则A为硝酸
B.若X为![]() 或
或![]() ,则A为硫酸
,则A为硫酸
C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1___ΔH2(填“>”“<”或“=”,下同)。
(2)相同条件下,1 molP4所具有的能量___4 molP原子所具有的能量。
(3)已知P4(白磷,s)4P(红磷,s) ΔH=-17kJ·mol-1,比较下列反应中ΔH的大小:ΔH1___ΔH2。
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2
(4)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则浓硫酸和稀氢氧化钠溶液反应生成2mol水,放出的热量___114.6kJ。
(5)已知:28gFe(s)与CO2(g)在一定条件下,完全反应生成FeO(s)和CO(g),吸收了akJ热量,该反应的热化学方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯的下列叙述:①能使酸性KMnO4溶液褪色②可发生加聚反应③可溶于水④可溶于苯中⑤苯环能与溴水发生取代反应⑥所有的原子可能共面。其中完全正确的是( )
A.①②④⑥
B.①②④⑤⑥
C.①②③④
D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2N2O5![]() 4NO2+O2开始时c(N2O5)=0.0408mol·L-1,经1 min后测得c(N2O5)=0.030mol·L-1,则该反应的反应速率为
4NO2+O2开始时c(N2O5)=0.0408mol·L-1,经1 min后测得c(N2O5)=0.030mol·L-1,则该反应的反应速率为
A. v(N2O5)=1.08×10-4 molL-1s-1 B. v(N2O5)= 1.8×10-1 molL-1min
C. v(O2)=9.0×10-5 molL-1s-1 D. 2 v(NO2)= v(N2O5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1984年,北京地坛医院成功研制了一种高效杀菌消毒试剂,此试剂后被命名为“84消毒液”。工业上,将氯气通入NaOH溶液可直接制得“84消毒液”。下列说法不正确的是
![]()
A.“84消毒液”的有效成分是NaClO
B.“84消毒液”能漂白棉、麻、纸张
C.“84消毒液”与酸性洁厕剂混用会产生Cl2
D.“84消毒液”久置失效,只涉及到氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
A. 原子数目相等的三种气体,质量最大的是Z
B. 同温同压下,同质量的三种气体,气体密度最小的是X
C. 若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 mol
D. 同温下,体积相同的两容器分别充2 g Y气体和1 g Z气体,则其压强比为2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g)![]() 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
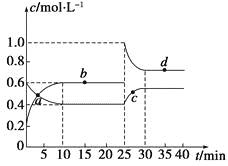
(1)该温度下,若温度升高,K值将________(填“增大”、“减小”或“不变”)。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是________点。从起点开始首次达到平衡时,以NO2表示的反应速率为____________。
(3)25 min时,加入了__________(填加入物质的化学式及加入的物质的量),使平衡发生了移动。
(4)d点对应NO2的物质的量浓度________(填“大于”、“小于”或“等于”)0.8 mol·L-1,理由是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com