
【题目】某固体粉末中可能含有SiO2、Fe2O3、CuO、NaHCO3、K2CO3 , 某同学设计并完成如下实验:(所加试剂均过量)已知:蘸取少量溶液2在酒精灯上灼烧,透过蓝色钴玻璃观察火焰呈紫色. 请回答: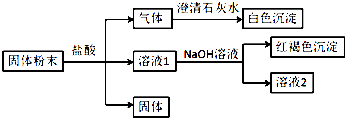
(1)白色沉淀是(填化学式).
(2)生成红褐色沉淀的离子方程式为 .
(3)根据实验现象,固体粉末中一定存在的组分是(填化学式).
【答案】
(1)CaCO3
(2)Fe3++3OH﹣=Fe(OH)3↓
(3)SiO2、Fe2O3、K2CO3
【解析】解:固体粉末中可能含有SiO2、Fe2O3、CuO、NaHCO3、K2CO3 , 由实验流程可知,加盐酸生成的气体能使石灰水变浑浊,则气体为CO2 , 溶液1与NaOH反应生成红褐色沉淀,沉淀为氢氧化铁,则原固体一定含Fe2O3 , 可知没有CuO,与盐酸反应后得到的固体为SiO2 , 又蘸取少量溶液2在酒精灯上灼烧,透过蓝色钴玻璃观察火焰呈紫色,为K的焰色反应,则原固体中含K2CO3 , (1)白色沉淀为二氧化碳与氢氧化钙反应生成的CaCO3 , 故答案为:CaCO3;(2分)(2)生成红褐色沉淀的离子方程式为Fe3++3OH﹣=Fe(OH)3↓,故答案为:Fe3++3OH﹣=Fe(OH)3↓;(3)由上述分析可知,一定含SiO2、Fe2O3、K2CO3 , 可能含NaHCO3 , 一定不含CuO,故答案为:SiO2、Fe2O3、K2CO3 . 固体粉末中可能含有SiO2、Fe2O3、CuO、NaHCO3、K2CO3 , 由实验流程可知,加盐酸生成的气体能使石灰水变浑浊,则气体为CO2 , 溶液1与NaOH反应生成红褐色沉淀,沉淀为氢氧化铁,则原固体一定含Fe2O3 , 可知没有CuO,与盐酸反应后得到的固体为SiO2 , 又蘸取少量溶液2在酒精灯上灼烧,透过蓝色钴玻璃观察火焰呈紫色,为K的焰色反应,则原固体中含K2CO3 , 以此来解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】欲配制100mL 1.0molL﹣1Na2SO4溶液,正确的方法是( )
①将7.1g Na2SO4溶于50mL水中
②将32.2g Na2SO410H2O晶体溶于少量水中,然后再用水稀释至100mL
③将25mL4.0molL﹣1Na2SO4溶液溶于75mL水中
④将50mL2.0molL﹣1Na2SO4溶液加入到40mL水中,然后再用水稀释至100mL.
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某盐的混合物中含有0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Clˉ,则SO42ˉ为( )
A.0.1mol/L
B.0.2mol/L
C.0.3mol/L
D.0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】艾薇醛(G,分子式:C9H14O)是一种新型的香料,可通过下列途径合成.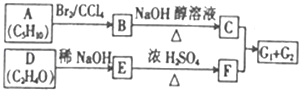
已知下列信息:
①A的核磁共振氢谱有3组峰,峰面积比为6:3:1
②A、C、F均能使Br2/CCl4溶液褪色
③D、E、F、G1、G2均能发生银镜反应,F中含甲基
④Diels﹣Alder反应(双烯合成反应).如: 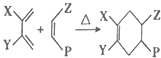
⑤ ![]()
回答下列问题:
(1)A的名称为;E→F的反应类型是 .
(2)B→C的化学方程式为 .
(3)D的结构简式为 .
(4)G1、G2(均含六元环)互为同分异构体,其结构简式分别为;
G1、G2在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是(填标号)
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(5)与E互为同分异构体且能发生银镜反应的异构体有种(不含立体结构,不含醚键),其中核磁共振氢谱有3组峰且面积比为6:1:1的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“固体干冰→液体二氧化碳→气体二氧化碳→气体一氧化碳”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、范德华力
B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式表示正确的是( )
A.碳酸钙与醋酸溶液反应:CaCO3+2H+=Ca2++CO2+H2O
B.苯酚钠溶液和少量CO2反应:2C6H5O﹣+CO2+H2O=2C6H5OH+CO32﹣
C.溴乙烷与氢氧化钠溶液共热:C2H5Br+OH﹣ ![]() C2H5OH+Br﹣
C2H5OH+Br﹣
D.用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH4)2++2OH﹣ ![]() CH3COO﹣+NH4++3NH3+2Ag↓+H2O
CH3COO﹣+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用含有少量氯化钙的氯化钠固体,配制100 mL 1mol·L-1的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题:
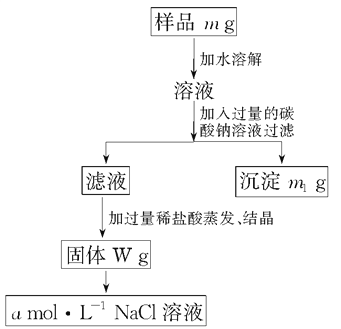
(1)称量粗盐样品m g,所用仪器名称为:_____________。
(2)过滤时,玻璃棒的作用是:__________________。
(3)蒸发操作时应将液体放在__________中加热,等加热至________时即停止加热。
(4)在样品的溶液中加入过量的Na2CO3溶液,作用是__________________,反应的化学方程式是______________________________________。
(5)在滤液中加入盐酸的作用是____________________________________,
反应的离子程式是_______________________________________。
(6)配制100 mL 1 mol·L-1的NaCl溶液时,应从W g固体中称取NaCl的质量为________,配制时应在________中进行定容。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验:

请回答下列问题:
(1)仪器a的名称是________________。
(2)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整_____。
(3)实验中他们取6.4g铜片和3mL8mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现娆瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:_______________________________;
实验中若有mg铜参加了反应,转移电子的数目为_______________。
②为什么有一定量的硫酸剩余但未能使铜片完全溶解? 你认为的原因是______________________。
③下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是_________(填写字母编号)。
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸氢钠固体
(4)为了测定剩余硫酸的物质的量,该兴趣小组通过分液漏斗加入过量的NaNO3溶液,测定烧瓶中产生的气体为物质的量之比为2∶1的NO和NO2混合气体,且完全反应后还有铜片剩余
①请写出加入NaNO3溶液后,容器中发生的离子方程式_______________________________。
②若实验中产生气体的总体积为336mL(标况下),则剩余硫酸的物质的量为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com