
【题目】在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2 (g)2SO3(g)(△H<0)
(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值 , 二氧化硫转化率 , 化学反应速率(以上均填增大、减小或不变).
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是 .
(4)据图判断,反应进行至20min时,曲线发生变化的原因是(用文字表达)
(5)10min到15min的曲线变化的原因可能是(填写编号).
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量.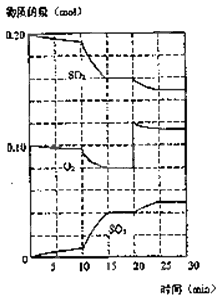
【答案】
(1)![]()
(2)增大;增大;减小
(3)15﹣20min和25﹣30min
(4)增大了氧气的浓度
(5)ab
【解析】解:(1)可逆反应2SO2(g)+O2 (g)2SO3(g)的平衡常数k= ![]() .所以答案是:
.所以答案是: ![]() .(2)该反应正反应为放热反应,降低温度平衡向正反应方向移动,平衡常数k增大,二氧化硫转化率增大,降低温度反应速率减小.
.(2)该反应正反应为放热反应,降低温度平衡向正反应方向移动,平衡常数k增大,二氧化硫转化率增大,降低温度反应速率减小.
所以答案是:增大、增大、减小.(3)反应混合物各物质的物质的量不变化,说明反应处于平衡状态,由图可知在15﹣20min和25﹣30min出现平台,各组分的物质的量不变,反应处于平衡状态.
所以答案是:15﹣20min和25﹣30min.(4)由图可知,反应进行至20min时,平衡向正反应移动,瞬间只有氧气的浓度增大,应是增大了氧气的浓度.
所以答案是:(5)由图可知,反应向正反应进行,10min到15min反应混合物单位时间内的变化量增大,说明反应速率增大,10min改变瞬间,各物质的物质的量不变.
a.加了催化剂,增大反应速率,故a正确;
b.缩小容器体积,增大压强,增大反应速率,故b正确;
c.降低温度反应速率降低,故c错误;
d.10min改变瞬间,各物质的物质的量不变,不是增加SO3的物质的量,故d错误.
故选:ab.
【考点精析】关于本题考查的化学平衡状态本质及特征,需要了解化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能得出正确答案.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.蔗糖不是淀粉水解的产物
B.蔗糖与麦芽糖互为同分异构体
C.蔗糖的水解产物能发生银镜反应
D.蔗糖是多羟基的醛类化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
A.9g甲基(﹣CH3)所含有的电子数是10 NA个
B.22.4L乙烷中含有的共价键数为7NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到相应实验目的是( )
A.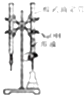 如图装置可用于已知浓度的氢氧化钠溶液滴定未知浓度的盐酸
如图装置可用于已知浓度的氢氧化钠溶液滴定未知浓度的盐酸
B.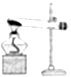 如图装置可用于氯化铵固体和氢氧化钙固体反应制取少量氨气
如图装置可用于氯化铵固体和氢氧化钙固体反应制取少量氨气
C.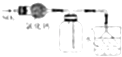 如图装置可用于收集SO2 , 并吸收多余的SO2
如图装置可用于收集SO2 , 并吸收多余的SO2
D. 如图装置可用于制取少量Cl2
如图装置可用于制取少量Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的类别完全正确的是( )
A. H2SO4,酸,电解质B. Al2O3,金属氧化物,非电解质
C. Na2CO3,碱,电解质D. CO2,酸性氧化物,电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与胶体性质无关的是( )
A. 明矾用作净水剂B. 在豆浆里加入盐卤做豆腐
C. 清晨在密林中看到缕缕光束D. 向三氯化铁溶液中加氢氧化钠溶液时产生红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( ) 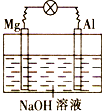
A.镁比铝活泼,镁失去电子被氧化成Mg2+
B.铝是电池负极,开始工作时溶液中会立即有白色沉淀生成
C.该装置的内、外电路中,均是电子的定向移动形成电流
D.该装置开始工作时,铝片表面的氧化膜可不必处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)和亚硫酰氯(SOCl2)均是实验室常见试剂.已知:
SO2Cl2(g)SO2(g)+Cl2(g) K1 △H=a kJ/mol (Ⅰ)
SO(g)+Cl(g)+SCl(g)2SOCl(g) K2 △H=b kJ/mol (Ⅱ)
(1)反应:SO2Cl2(g)+SCl(g)2SOCl2(g)的平衡常数K=(用K1、K2表示),该反应△H=kJ/mol(用a、b表示).
(2)为研究不同条件对反应(Ⅰ)的影响,以13.5g SO2Cl2充入2.0L的烧瓶中,在101kPa 375K时,10min达到平衡,平衡时SO2Cl2转化率为0.80,则0~10minCl2的平衡反应速率为 , 平衡时容器内压强为 kPa,该温度的平衡常数为;若要减小SO2Cl2转化率,除改变温度外,还可采取的措施是(列举一种).
(3)磺酰氯对眼和上呼吸道粘膜有强烈的刺激性,发生泄漏时,实验室可用足量NaOH固体吸收,发生反应的化学方程式为;亚硫酰氯溶于水的离子方程式为 .
(4)一定量的Cl2用稀NaOH溶液吸收,若恰好反应,则溶液中各离子浓度由大到小的顺序为;已知常温时次氯酸的Ka=2.5×10﹣8则该温度下NaClO水解反应的平衡常数Kb=molL﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com