
【题目】A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液中,现象为出现白色沉淀→灰绿色沉淀→红褐色沉淀E.试推断:
(1)B:、E:
(2)①C加热分解的化学方程式: ②A与无色无味气体反应的离子方程式:
③由白色沉淀最终变为红褐色沉淀E的化学方程式: .
【答案】
(1)KOH;Fe(OH)3
(2)2NaHCO3 ![]() Na2CO3+CO2↑+H2O;CO32﹣+CO2+H2O=2HCO3﹣;2Fe(OH)2+O2+2H2O=4Fe(OH)3
Na2CO3+CO2↑+H2O;CO32﹣+CO2+H2O=2HCO3﹣;2Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】解:、C、D焰色反应均为黄色,说明都含有钠元素的化合物;B是碱且透过钴玻璃观察焰色反应为紫色,判断为含K元素,A、C和盐酸反应均得到D的溶液,D为NaCl,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,可以判断,无色无味的气体是CO2 , A为Na2CO3 , C为NaHCO3 , 若B的溶液滴加到硫酸亚铁溶液中,现象为出现白色沉淀→灰绿色沉淀→红褐色沉淀E,白色沉淀为Fe(OH)2 , 则B为KOH,E为Fe(OH)3 , (1)由以上分析可知B为KOH,E为Fe(OH)3 , 所以答案是:KOH;Fe(OH)3;(2)①C为NaHCO3 , 不稳定,加热易分解,反应的方程式为2NaHCO3 ![]() Na2CO3+CO2↑+H2O,所以答案是:2NaHCO3
Na2CO3+CO2↑+H2O,所以答案是:2NaHCO3 ![]() Na2CO3+CO2↑+H2O;②A为Na2CO3 , 与二氧化碳反应生成碳酸氢钠,反应的离子方程式为CO32﹣+CO2+H2O=2HCO3﹣ , 所以答案是:CO32﹣+CO2+H2O=2HCO3﹣;③白色沉淀Fe(OH)2最终变为红褐色沉淀E的化学方程式为2Fe(OH)2+O2+2H2O=4Fe(OH)3 , 所以答案是:2Fe(OH)2+O2+2H2O=4Fe(OH)3 .
Na2CO3+CO2↑+H2O;②A为Na2CO3 , 与二氧化碳反应生成碳酸氢钠,反应的离子方程式为CO32﹣+CO2+H2O=2HCO3﹣ , 所以答案是:CO32﹣+CO2+H2O=2HCO3﹣;③白色沉淀Fe(OH)2最终变为红褐色沉淀E的化学方程式为2Fe(OH)2+O2+2H2O=4Fe(OH)3 , 所以答案是:2Fe(OH)2+O2+2H2O=4Fe(OH)3 .


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】a、b代表2种金属,下列叙述中,肯定能判断金属活动性a比b强的是( )
A. 常温下,a能从水中置换出氢,而b不能 B. 原子的电子层数a比b多
C. 原子的最外层电子数a比b少 D. 1 mol a 、b分别与足量盐酸反应,生成H2的质量a比b大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
![]()
试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子方程式为_________________;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有__________、玻璃棒和烧杯等;步骤Ⅳ中最好应选用_______试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氧化铜 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是_____________________;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是______________________;
(5)步骤Ⅵ中发生反应的化学反应方程式为_______________________________;
(6) 欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: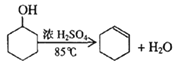


(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入块状物质,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①块状物质的作用是___________,导管B的作用是___________。
②试管C置于冰水浴中的目的是____________________________________。

(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从_______口流出,目的是_________
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___________
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_______________________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧产生的粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是火电厂产生的废渣,若不加处理会污染环境。为综合利用,研究人员对其进行如下处理:

(1)滤渣主要成分是________________;滤液①中的阳离子为_____________________。
(2)滤液①中还加入还原剂原因是________________;若加入的还原剂为铁粉,反应的离子方程式为_____________________________________。
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为_________________;反应终点的pH对铝和铁分离效果的影响如右图。根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是__________,选择该范围的理由是_________。

(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是_____________。
②煅烧NH4Al(SO4)2时发生4NH4Al(SO4)2![]() 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O)。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________(填化学式);试剂Y是_________(填名称),其中溶质的物质的量为_____________。
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O)。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________(填化学式);试剂Y是_________(填名称),其中溶质的物质的量为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 碱金属元素最外层电子数都是1个,化学性质均活泼
B. 碱金属元素从上到下随电子层数的增多金属性依次增强
C. 碱金属元素的单质都是银白色的,都比较柔软
D. 碱金属元素的单质从上到下熔沸点逐渐降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20mL 0.5mol/L的盐酸与一块大理石反应,下列措施不能提高反应速率的是 ( )
A. 加入10mL 1mol/L的盐酸 B. 加入30mL 10mol/L的盐酸
C. 加入10mL H2O D. 所用的大理石研磨成粉末
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决能源危机,在汽油中掺入一定比例的乙醇(即“乙醇汽油”),以代替一部分汽油。乙醇在气缸中完全燃烧的热化学方程式为:
![]() C2H5OH(l)+
C2H5OH(l)+![]() O2(g)=CO2(g)+
O2(g)=CO2(g)+![]() H2O(l) △H1=-683.4 kJ/mol
H2O(l) △H1=-683.4 kJ/mol
下列说法正确的是
A.该反应过程中,断裂化学键会放出热量
B.该反应中,生成物的总能量大于反应物的总能量
C.乙醇的燃烧热为683.4 kJ/mol
D.反应![]() C2H5OH(l)+
C2H5OH(l)+![]() O2(g)=CO2(g)+
O2(g)=CO2(g)+![]() H2O(g)的△H2>-683.4 kJ/mol
H2O(g)的△H2>-683.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一块11.0g的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加H2O2到溶液中无Fe3+存在,加热除去多余的H2O2 , 当加入200mL 6molL﹣1NaOH溶液时沉淀量最多,且所得沉淀质量为26.3g,下列说法不正确的是( )
A.该合金中铁的质量为5.6g
B.合金与稀硫酸反应共生成0.45mol H2
C.该合金与足量氢氧化钠反应,转移的电子数为0.6NA
D.所加的稀硫酸中含0.6molH2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com