
 消除大气污染有多种方法.
消除大气污染有多种方法.| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
分析 (1)利用盖斯定律②×2-①+③×2得到热化学反应方程式;
(2)Fe3+被SO2还原成Fe2+,接着Fe2+再被氧气氧化成Fe3+;
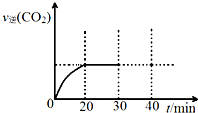
(3)①根据v=$\frac{△c}{△t}$计算v(CO2)
②20min处于平衡状态,根据K=$\frac{c({N}_{2})×c(C{O}_{2})}{{c}^{2}(NO)}$计算平衡常数;
③一定温度下,随着NO的起始浓度增大,等效为增大压强,不影响平衡移动;
④30min~40min之间,NO浓度减小0.08mol/L,N2浓度增大0.04mol/L,CO2浓度减小0.13mol/L,应是减小二氧化碳的浓度,瞬间减小二氧化碳的浓度为(0.3+0.04)mol/L-0.17mol/L=0.17mol/L,平衡时浓度为0.17mol/L.
解答 解:(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+2NO2(g)═N2 (g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
利用盖斯定律②×2-①+③×2得到热化学反应方程式:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)△H=-1248 kJ•mol-1,
故答案为:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)△H=-1248 kJ•mol-1;
(2)Fe3+被SO2还原成Fe2+,接着Fe2+再被氧气氧化成Fe3+,离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,
故答案为:4Fe2++O2+4H+═4Fe3++2H2O;
(3)①10min~20min以v(CO2) 表示的反应速率=$\frac{(0.3-0.21)mol•{L}^{-1}}{(20-10)min}$=0.009 mol•L-1•min-1,
故答案为:0.009 mol•L-1•min-1;
②20min处于平衡状态,平衡常数K=$\frac{c({N}_{2})×c(C{O}_{2})}{{c}^{2}(NO)}$=$\frac{0.3×0.3}{0.{4}^{2}}$=0.56,
故答案为:0.56;
③一定温度下,随着NO的起始浓度增大,等效为增大压强,不影响平衡移动,则NO的平衡转化率不变,
故答案为:不变;
④30min~40min之间,NO浓度减小0.08mol/L,N2浓度增大0.04mol/L,CO2浓度减小0.13mol/L,应是减小二氧化碳的浓度,瞬间减小二氧化碳的浓度为(0.3+0.04)mol/L-0.17mol/L=0.17mol/L,该瞬间二氧化碳浓度为0.13mol/L,平衡时浓度为0.17mol/L,则30min至40minCO2浓度的变化曲线图象为: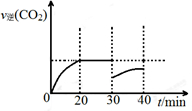 ,
,
故答案为: .
.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、平衡常数、反应速率、热化学方程式书写等,(3)中作图为易错点,注意二氧化碳的瞬间浓度与平衡浓度.


科目:高中化学 来源: 题型:选择题
| A. | 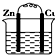 CuSO4溶液 | B. | 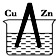 ZnSO4溶液 | ||
| C. | 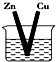 酒精 | D. | 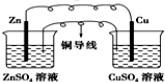 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | 30 | 30 | 30 | 30 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | 20 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
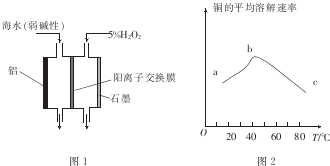
| 实验 体积/mL 液体 | A | B | C | D |
| 0.4mol.L-1Fe2(SO4)3溶液 | 0 | 1.8 | 2.0 | V1 |
| 30%H2O2溶液 | 20.0 | 20.0 | 20.0 | 20.0 |
| HO2 | V2 | V3 | 15.0 | 13.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素是典型的非金属元素,因此不能与其他非金属元素化合 | |
| B. | 卤素单质越活泼,其熔、沸点就越高 | |
| C. | 卤素单质都能和水剧烈反应 | |
| D. | 卤素单质都能和H2反应,且气态氢化物的稳定性随单质氧化性的增强而增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
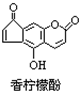
| A. | 它的分子式为C13H9O4 | |
| B. | 它与H2发生加成反应,1mol最多可消耗7mol H2 | |
| C. | 它与溴水发生反应,1mol最多消耗3mol Br2 | |
| D. | 它与NaOH溶液反应,1mol最多消耗2molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
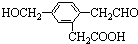 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤ | D. | ①③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com